Questão 13
(EsPCEx - 2009)
Assinale a alternativa correta:
A condutividade elétrica dos metais é explicada admitindo-se a existência de nêutrons livres.
O nitrato de sódio é um composto iônico, mas que apresenta ligações covalentes entre o átomo de nitrogênio e os átomos de oxigênio.
Uma molécula com ligações polares pode somente ser classificada, quanto à sua polaridade, como uma molécula polar.
Não existe força de atração entre moléculas apolares.
As forças de atração entre as moléculas do ácido bromídrico são denominadas ligações de hidrogênio.
Gabarito:
O nitrato de sódio é um composto iônico, mas que apresenta ligações covalentes entre o átomo de nitrogênio e os átomos de oxigênio.
Resolução:
Analisando as alternativas:
A) [INCORRETA] Pois as ligas metálicas são caracterizadas pela presença de elétrons livres. Além disso, ânions (como composto do núcleo do átomo) não se desprendem, a não ser por radiação
B) [CORRETA] Pois o nitrato de sódio NaNO3 é um composto iônico (Na+ e NO3-) em que os átomos do ânion nitrato realizam ligação covalente.
C) [INCORRETA] Pois se a molécula for formada por três átomos ou mais, deve-se analisar cada ligação, pois o momento dipolo () dado pela soma vetorial pode ser nulo, mesmo que existam ligações polares.
Ex.:
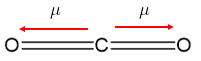
D) [INCORRETA] Pois moléculas apolares realizam interações dipolo induzido - dipolo induzido (forças de London ou forças de dispersão).
E) [INCORRETA] Pois o ácido brómico (HBr) realiza ligação dipolo-dipolo.
Obs.: Ligações de hidrogênio ocorrem em moléculas que tenham hidrogênio ligando a flúor, nitrogênio e oxigênio.
.png)