Questão 62510
(FCM 2015)
Muitas são as teorias existentes para explicar as ligações entre os elementos químicos como a teoria de ligação de valência (associada ao modelo da hibridização) e a teoria do orbital molecular. Estas teorias são propostas diferentes para descrever a estrutura molecular baseadas no modelo da mecânica quântica. Assim a existência de orbitais atômicos dando origem a orbitais moleculares, sua distribuição espacial, ângulos e comprimentos de ligação e a geometria de uma molécula são melhor compreendidos e explicados utilizando a teoria quântica. Baseando-se nestas teorias de ligação entre os elementos químicos, é correto afirmar que:
a molécula do BF3 apresenta 3 ligações utilizando orbitais moleculares s–sp2.
a molécula de H2O apresenta 2 orbitais moleculares s–sp3.
a molécula do C2H4 apresenta geometria molecular tetraédrica.
a molécula do SO3 apresenta ângulos de ligação menores que 120º.
a molécula do gás N2 apresenta dois orbitais moleculares sigma do tipo p–p.
Gabarito:
a molécula de H2O apresenta 2 orbitais moleculares s–sp3.
Resolução:
a) Incorreto. a molécula do BF3 apresenta 3 ligações utilizando orbitais moleculares s–sp2.
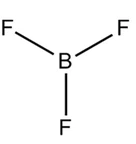
Átomo Central: B
3 ligações sigma: s p p = sp2, F também vai possuir orbital p e não s.
b) Correto. a molécula de H2O apresenta 2 orbitais moleculares s–sp3.
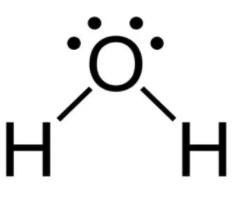
O Oxigênio faz 2 ligações sigma e possui 2 pares de elétrons livres: sp3, o H é orbital s.
c) Incorreto. a molécula do C2H4 apresenta geometria molecular tetraédrica.
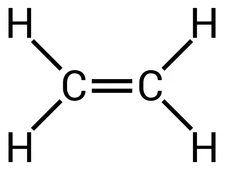
Geometria trigonal planar.
d) Incorreto. a molécula do SO3 apresenta ângulos de ligação menores que 120º.
Maiores:
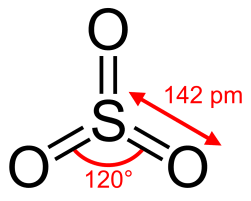
e) Incorreto. a molécula do gás N2 apresenta dois orbitais moleculares sigma do tipo p–p.
Há hibridação, portanto possui orbital hibrido, e não molecular