Questão 9306
(FUVEST 2000)
Propriedades de algumas substâncias:
| Substância | Ponto de fusão (ºC) | Solubilidade a 25ºC em água (g/100cm3) | Solubilidade a 25ºC em CCl4 (g/100cm3) | Densidade a 25ºC (g/cm3) |
| Água | 0,0 | - | ≈ 0 | 1,00 |
| Iodo | 113,5 | 0,03 | 2,90 | 4,93 |
| CCl4 | -23,0 | ≈ 0 | - | 1,59 |
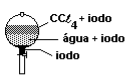
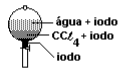
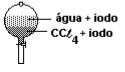
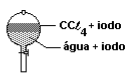
A 25 °C, 3,00 g de iodo, 70 cm3 de água e 50 cm3 de CCℓ4 são colocados em um funil de separação. Após agitação e repouso, qual dos esquemas seguir deve representar a situação final?
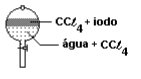
Gabarito:

Resolução:
Pela tabela concluímos que água e CCl4 não são miscíveis. Pela densidade, teremos, de cima para baixo, água, CCl4 , (Iodo) se houver precipitação, caso não seja possível ser totalmente solubilizado.
A solubilidade do Iodo em CCl4 é 2,9g por 100cm3. Como temos 70cm3, só será solubilizado 2,03g em clorofórmio. Em água, a solubilidade é 0,03g por 100cm3, então só possível solubilizar em água 0,021g de I2. A soma da massa de iodo solubilizada nos dois solventes é igual a 2,051g, menor que os 3g de iodo adicionado, portanto, terá corpo de fundo.
2,9g de iodo -> 100cm3 de clorofórmio
xg -> 50cm3
x=1,45g
0,03g de iodo -> 100cm3 de água
xg -> 70cm3
x=0,021g