Questão 44847
(FUVEST - 2006)
Industrialmente, HCl gasoso é produzido em um maçarico, no qual entram, nas condições-ambiente, hidrogênio e cloro gasosos, observando-se uma chama de vários metros de altura, proveniente da reação entre esses gases.
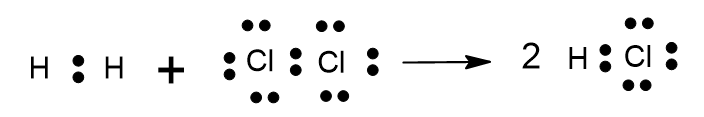
a) Escreva a equação química que representa essa transformação, utilizando estruturas de Lewis tanto para os reagentes quanto para o produto.
b) Como se obtém ácido clorídrico a partir do produto da reação de hidrogênio com cloro? Escreva a equação química dessa transformação.
c) Hidrogênio e cloro podem ser produzidos pela eletrólise de uma solução concentrada de cloreto de sódio (salmoura). Dê as equações que representam a formação de cada um desses gases.
d) Que outra substância é produzida, simultaneamente ao cloro e ao hidrogênio, no processo citado no item anterior?
|
Número atômico (Z) hidrogênio..............1 cloro.....................17 |
Gabarito:
Resolução:
a) Escreva a equação química que representa essa transformação, utilizando estruturas de Lewis tanto para os reagentes quanto para o produto.
b) Como se obtém ácido clorídrico a partir do produto da reação de hidrogênio com cloro? Escreva a equação química dessa transformação.
c) Hidrogênio e cloro podem ser produzidos pela eletrólise de uma solução concentrada de cloreto de sódio (salmoura). Dê as equações que representam a formação de cada um desses gases.
Dissociação do cloreto de sódio: NaCl(s) → Na+(aq) + Cl-(aq)
Reação anódica: 2 Cl-(aq) → Cl2(g) + 2e-
Reação catódica: 2 H2O(l) + 2e- → H2(g) + 2 OH-(aq)
d) Que outra substância é produzida, simultaneamente ao cloro e ao hidrogênio, no processo citado no item anterior?
Somando as equações, encontramos a reação de formação do NaOH partindo da eletrólise do NaCl.
2NaCl + 2H2O → H2 + Cl2 + 2NaOH