Questão 44915
(FUVEST 2008 - 2ª fase) Em um exame, para o preenchimento de uma vaga de químico, as seguintes fórmulas estruturais foram apresentadas ao candidato:
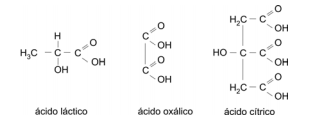
A seguir, o examinador pediu ao candidato que determinasse, experimentalmente, o calor liberado ao fazer-se a mistura de volumes definidos de duas soluções aquosas, de mesma concentração, uma de hidróxido de sódio e outra de um dos três ácidos carboxílicos apresentados, sem revelar qual deles havia sido escolhido. Foi informado ao candidato que, quando o ácido e a base reagem na proporção estequiométrica, o calor liberado é máximo.
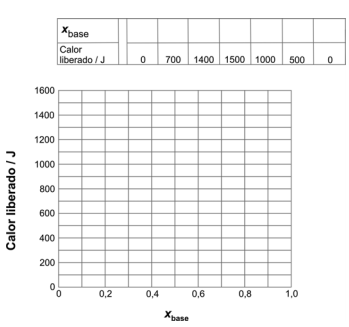
Os resultados obtidos foram os seguintes:

Diante dos resultados obtidos, o examinador pediu ao candidato que determinasse qual dos ácidos havia sido utilizado no experimento. Para responder, o candidato construiu uma tabela e um gráfico do calor liberado versus xbase, definido como:
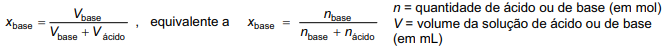
a) Reproduza, na página ao lado, a tabela e o gráfico que devem ter sido obtidos pelo candidato. Pelos pontos do gráfico, podem ser traçadas duas retas, cujo cruzamento corresponde ao máximo calor liberado.
b) Determine o valor de que corresponde ao ponto de cruzamento das retas em seu gráfico.
c) Qual foi o ácido escolhido pelo examinador? Explique.
d) Indique qual é o reagente limitante para o experimento em que o calor liberado foi 1400 J e para aquele em que o calor liberado foi 1500 J. Explique.
Gabarito:
Resolução:
a) 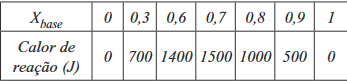
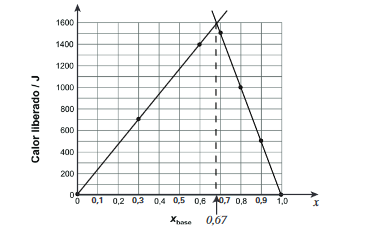
b) Para obter esse valor, utilizamos as equações de cada reta, de forma que:
y = (1400/0,6) . x y = (– 1000/ 0,2) . x + 1000/0,2
A partir dessas equações, podemos determinar que no ponto de encontro temos x = 0,67.
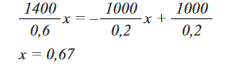
c) O valor de x no ponto de encontro equivale ao calor máximo liberado na reação de neutralização, de forma que podemos estabelecer uma proporção de aproximadamente 2:1 entre base e ácido:
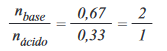
Sendo assim, se cada 2 mols de base são gastos para cada mol de ácido, podemos concluir que esse ácido possui 2 hidrogênios ionizáveis, ou seja, o ácido oxálico.
d) Para uma quantidade de calor liberado igual a 1400 J, o ácido estará em excesso, devido a proporção entre base e ácido de 1: 2. Já para uma quantidade de calor liberado igual a 1500 J, a
base estará em excesso.