Questão 44921
(FUVEST 2008 - 2ª fase) Foi montada uma pilha em que o pólo positivo era constituído por um bastão de paládio, mergulhado numa solução de cloreto de paládio e o pólo negativo, por um bastão de níquel, mergulhado numa solução de sulfato de níquel. As semi-reações que representam os eletrodos são:
a) Escreva a equação que representa a reação química que ocorre quando a pilha está funcionando (sentido espontâneo).
b) O que acontece com as concentrações de e
durante o funcionamento da pilha? Explique.
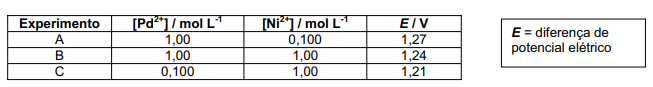
c) Os dados da tabela abaixo sugerem que o princípio de Le Châtelier se aplica à reação química que acontece nessa pilha. Explique por quê.
Gabarito:
Resolução:
a) Ni + Pd2+ → Ni2+ + Pd
b) A partir da reação global, podemos afirmar que Pd2+ tem sua concentração diminuída, pois está sendo consumido como reagente pela reação, enquanto Ni2+ aumenta sua concentração, já que é um produto.
c) O principio se aplica a essa reação pois a concentração de íons Ni2+ aumenta do experimento A para o experimento B, onde a diferença de potencial elétrico diminui já que o equilíbrio é deslocado para
a esquerda. A concentração de íons Pd2+, assim como anteriormente, diminui do experimento B para o experimento C, diminuindo a diferença de potencial elétrico já que o equilíbrio é deslocado para a esquerda, mantendo a concentração de íons Ni 2+ constante.