Questão 2
(FUVEST - 2009 - 2 fase - Questão 2)
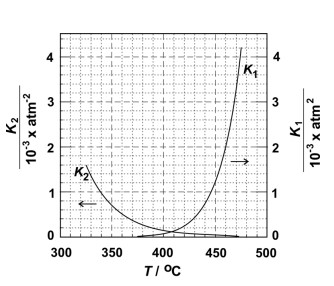
A reforma do gás natural com vapor de água é um processo industrial de produção de hidrogênio, em que também se gera monóxido de carbono. O hidrogênio, por sua vez, pode ser usado na síntese de amônia, na qual reage com nitrogênio. Tanto a reforma do gás natural quanto a síntese da amônia são reações de equilíbrio. Na figura, são dados os valores das constantes desses equilíbrios em função dos valores da temperatura. A curva de K1 refere-se à reforma do gás natural e a de K2, à síntese da amônia. As constantes de equilíbrio estão expressas em termos de pressões parciais, em atm.
a) Escreva a equação química balanceada que representa a reforma do principal componente do gás natural com vapor de água.
b) Considere um experimento a 450 C o , em que as pressões parciais de hidrogênio, monóxido de carbono, metano e água são, respectivamente, 0,30; 0,40; 1,00 e 9,00 atm. Nessas condições, o sistema está em equilíbrio químico? Justifique sua resposta por meio de cálculos e análise da figura.
c) A figura permite concluir que uma das reações é exotérmica e a outra, endotérmica. Qual é a reação exotérmica? Justifique sua resposta.
Gabarito:
Resolução:
a) CH4(g) + H2O(g) --> CO(g) + 3H2(g)
b) Para que esse sistema esteja em equilíbrio químico é necessário que o valor da constante de equilíbrio (Kp= 1,2 . 10-3) seja o mesmo que o do quociente reacional Qp na temperatura fornecida. Sendo assim, utilizaremos as pressões parciais fornecidas para realizar o cálculo, assim como demonstrado:
Qp =
Como Qp = Kp, podemos afirmar que o sistema está em equilíbrio.
c) Em uma reação exotérmica, o aumento da temperatura causa a diminuição da constante de equilíbrio, de forma que o equilíbrio irá se deslocar no sentido da reação que precisa de calor. A partir disso podemos concluir que a reação exotérmica é a da amônia:
N2(g) + 3H2(g) --> 2NH3(g) (K2)