Questão 70
(FUVEST - 2009 - 1 FASE)
Considere uma solução aquosa diluída de ácido acético (HA), que é um ácido fraco, mantida a 25ºC. A alternativa que mostra corretamente a comparação entre as concentrações, em mol/L, das espécies químicas presentes na solução é
Dados, a 25ºC : Constante de ionização do HA:
Produto iônico da água:
Constantes de equilíbrio com concentrações em mol/L
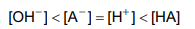
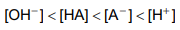
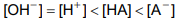
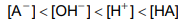
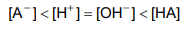
Gabarito:
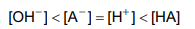
Resolução:
A reação de ionização do ácido acético pode ser representada por:
HA ⇌ H+ + A–
• A questão informa que o ácido acético (HA) é um ácido fraco, portanto, ioniza pouco. Então a concentração de HA vai ser maior que a de H+.
• Como a proporção estequiométrica entre H+ e A– é de 1 : 1, pode-se considerar que as suas concentrações serão iguais.
• Como a constante de ionização (Ka) do ácido acético é maior do que o produto iônico da água (Kw), a concentração de A– é maior que a de OH–.
A ordem correta é:
OH- < A- = H+ < HA