Questão 10
(FUVEST - 2009 - 2 fase - Questão 10)
Pilocarpina (P) é usada no tratamento do glaucoma. Em meio alcalino, sofre duas reações simultâneas: isomerização, formando iso-pilocarpina (i-P) e hidrólise, com formação de pilocarpato (). Em cada uma dessas reações, a proporção estequiométrica entre o reagente e o produto é de 1 para 1.
Num experimento, a 25ºC, com certa concentração inicial de pilocarpina e excesso de hidróxido de sódio, foram obtidas as curvas de concentração de i-P e PA em função do tempo, registradas no gráfico. Considere que, decorridos 200 s, a reação se completou, com consumo total do reagente pilocarpina.
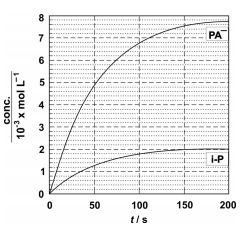
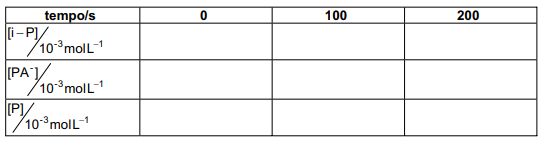
a) Para os tempos indicados na tabela da folha de respostas, complete a tabela com as concentrações de i-P e .
b) Complete a tabela com as concentrações do reagente P.
c) Analisando as curvas do gráfico, qual das duas reações, a de isomerização ou a de hidrólise, ocorre com maior velocidade? Explique.
Gabarito:
Resolução:
a) De acordo com a leitura do gráfico:
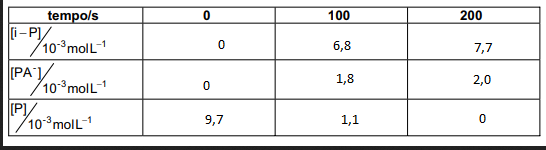
b) Utilizando a tabela preenchida anteriormente, obtemos as seguintes concentrações:
1 mol de P –––––– 1 mol de PA –
x –––––– 7,7 . 10 –3 mol de PA–
x = 7,7 . 10–3 mol de P
1 mol de P –––––– 1 mol de i-P
y –––––– 2,0 . 10–3 mol de i-P
y = 2,0 . 10–3 mol de P
Concentração de P no instante zero:
x + y = (7,7 . 10–3) + (2,0 . 10–3) = 9,7 . 10–3 mol/L
c) Considerando um mesmo intervalo de tempo, observamos uma maior quantidade (mols) de PA – (hidrólise) do que de i-P (isomerização). Logo, a hidrólise tem maior velocidade de reação.