Questão 1
(FUVEST - 2010 - 2 fase - Questão 1)
O sólido pode decompor-se, reversivelmente, em cloreto de magnésio e amônia. A equação química que representa esse processo é:
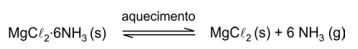
Ao ser submetido a um aquecimento lento, e sob uma corrente de nitrogênio gasoso, o sólido perde massa, gradativamente, como representado no gráfico:
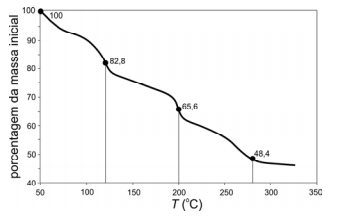
As linhas verticais, mostradas no gráfico, delimitam as três etapas em que o processo de decomposição pode ser dividido.
a) Calcule a perda de massa, por mol de , em cada uma das três etapas.
b) Com base nos resultados do item anterior, escreva uma equação química para cada etapa de aquecimento. Cada uma dessas equações deverá representar a transformação que ocorre na etapa escolhida.
c) No processo descrito, além do aquecimento, que outro fator facilita a decomposição do ? Explique.
Dados: massa molar (g/mol):
....... 197
............................ 17,0
Gabarito:
Resolução:
a) O gráfico da questão apresenta os dados da massa em porcentagem, podemos considerar que 1 mol corresponde à massa inicia e que a perda de massa em cada etapa foi subtraída daquela da etapa anterior.
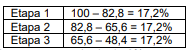
17,2% de 197g é 33,9g
b) A massa perdida em cada etapa se deve a perda de amônia com o aquecimento até que fique apenasapenas o MgCl2. Com massa molar de, 17,0 g/mol temos aproximadamente de 2 mol eliminados. Desta forma, em cada etapa há a perda de duas moléculas de amônia:
| Etapa 1 | |
| Etapa 2 | |
| Etapa 3 |
c) A corrente de nitrogênio gasoso facilita a decomposição do MgCl2·6NH3, porque a corrente deste gás inerte retira a amônia gasosa por arraste. A diminuição da concentração do produto, no caso a amônia, leva a um deslocamento do equilíbrio no sentido de maior formação deste, e consequentemente maior decomposição.