Questão 44585
(FUVEST - 2011)
Em um funil de separação, encontram-se, em contato, volumes iguais de duas soluções: uma solução aquosa de I2, de concentração 0,1*10-3 mol/L, e uma solução de I2 em CCl4, de concentração 1,0*10-3 moI/L.
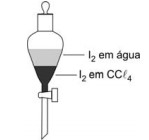
Considere que o valor da constante Kc do equilíbrio é igual a 100, à temperatura do experimento, para concentrações expressas em moI/L. Assim sendo, o que é correto afirmar a respeito do sistema descrito?
I2(aq) ⇌ I2(CCl4)
Se o sistema for agitado, o I2 será extraído do CCl4 pela água, até que a concentração de I2 em CCl4 se iguale a zero.
Se o sistema for agitado, o I2 será extraído da água pelo CCl4, até que a concentração de I2 em água se iguale a zero.
Mesmo se o sistema não for agitado, a concentração de I2 no CCl4 tenderá a aumentar e a de I2, na água, tenderá a diminuir, até que se atinja um estado de equilíbrio.
Mesmo se o sistema não for agitado, a concentração de I2 na água tenderá a aumentar e a de I2, no CCl4, tenderá a diminuir, até que se atinja um estado de equilíbrio.
Quer o sistema seja agitado ou não, ele já se encontra em equilíbrio e não haverá mudança nas concentrações de I2 nas duas fases.
Gabarito:
Mesmo se o sistema não for agitado, a concentração de I2 no CCl4 tenderá a aumentar e a de I2, na água, tenderá a diminuir, até que se atinja um estado de equilíbrio.
Resolução:
O quociente de equilíbrio (Q) para a reação I2(g) ⇌ I2(CCl4) pode ser calculado por:
Substituindo os valores fornecidos na questão de concentração, temos que:
Como o valor de Q é menor que o de Kc (Kc = 100) o equilíbrio vai estar deslocado para a direita até que se atinja o equilíbrio, independente de agitação ou não. Portanto, com o equilíbrio deslocado para a direita, a concentração de I2(aq) vai diminuir e a de I2(CCl4) vai aumentar.
Gabarito é a alternativa C.