Questão 2
(FUVEST - 2023)
O diamante, uma estrutura cristalina de carbono, é o material mais duro encontrado na natureza. Mastigar diamantes provavelmente quebraria os dentes e a sua ingestão causaria desconforto. Entretanto, há uma forma extravagante de ingerir um diamante, que é utilizá-lo para produzir água com gás, como no seguinte procedimento:
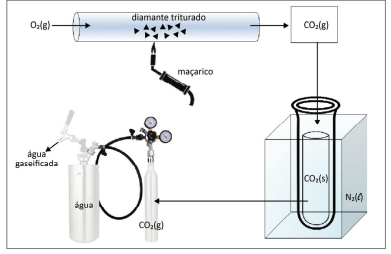
1 – O diamante triturado foi inserido dentro de um tubo de vidro;
2 – Foi injetado oxigênio gasoso no tubo de vidro, que foi aquecido com um maçarico;
3 – O gás produzido foi recolhido dentro de um tubo de ensaio imerso em nitrogênio líquido;
4 – Todo o sólido formado dentro do tubo de ensaio foi transferido para um cilindro de gás de volume interno de 1 L com a válvula fechada. Todo o CO2 sublimou dentro desse cilindro;
5 – O cilindro de gás foi então conectado a uma garrafa de água, que foi gaseificada com a abertura da válvula do cilindro.
a) Com base no esquema, a temperatura de fusão do N2 é maior, menor ou igual a temperatura de fusão do CO2?
b) Se um experimento exatamente igual for realizado trocando o volume de diamante utilizado pelo mesmo volume de grafite, a quantidade de CO2 formado ao fim do processo será menor, igual ou maior? Explique.
c) Partindo-se de 3 g de diamante, qual a massa de gelo seco obtida? Qual será a pressão gerada pelo CO2(g) dentro do cilindro de gás a 27 °C? Considere que o rendimento do experimento é de 100%.
Note e adote:
Densidade (g/cm3): Grafite = 2,0; Diamante = 3,5.
Massas molares (g/mol): C = 12; O = 16.
Constante universal dos gases ideais: .
Gabarito:
Resolução:
a) A temperatura em que o nitrogênio (N2) muda do estado sólido para o líquido é mais baixa do que a temperatura em que o dióxido de carbono (CO2) faz essa transição. Isso acontece porque a solidificação do CO2 é influenciada pelo nitrogênio no estado líquido.
b) Se a densidade é maior, a massa também será maior. Ao substituir o diamante (densidade de 3,5 g/cm³) pelo grafite (densidade de 2,0 g/cm³) com o mesmo volume, haverá uma menor quantidade de dióxido de carbono presente, pois o grafite possui uma massa de carbono inferior.
c) Quantidade de mols de gelo seco produzidos:
A equação é Cdiamante + O2 → CO2
Como 1 mol de carbono produz 1 mol de CO2, podemos fazer a relação
, logo, x = 0,25 mol de CO2 produzido.
Com os dados fornecidos, podemos calcular a preção pela equação de Clayperon
pV=nRT ⇒ p·(1L) = (0,25 mol)(0,082 atm.L.mol–1.K–1)((27+273) K) ⇒ p = 6,15 atm