Questão 6
(FUVEST - 2023)
Um processo típico de adulteração do leite envolve uma simples diluição com água. Essa adulteração pode ser avaliada pela quantidade de proteína na amostra. Segundo pesquisadores do CENA-USP (Centro de Energia Nuclear na Agricultura da Universidade São Paulo), as proteínas do leite podem ser precipitadas com sulfato de cobre em meio salino por efeito dos íons Cu2+. Pela quantidade de Cu2+ remanescente em solução, é possível calcular, por diferença, a quantidade de proteína na amostra.
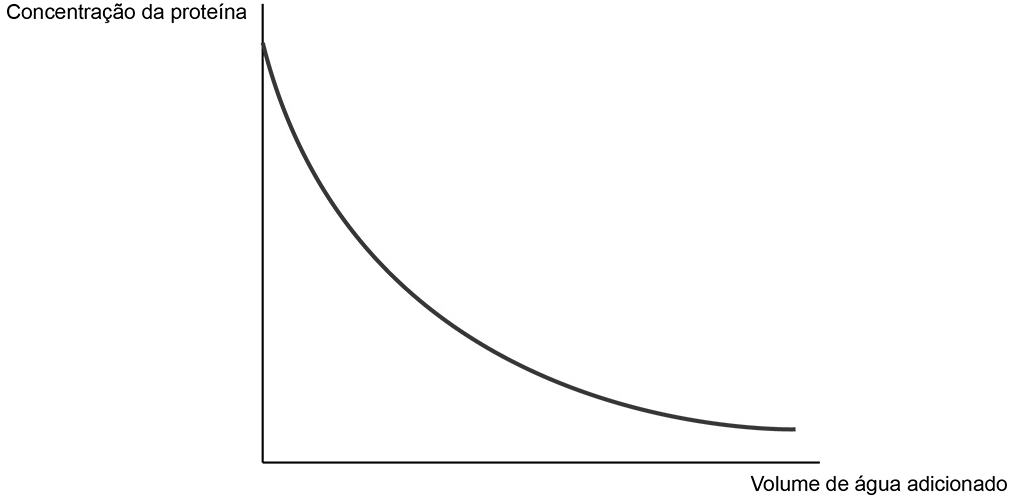
a) Esboce, na folha de respostas, um gráfico da variação da concentração de proteína em função do volume de água adicionado ao leite.
b) Suponha que uma amostra de 1L de leite não adulterado foi tratada com uma certa quantidade de sulfato de cobre, de modo que toda a proteína presente na amostra fosse precipitada. Se essa mesma quantidade de sulfato de cobre for utilizada em 1L de uma amostra de leite adulterado por diluição, a solução remanescente terá menor, maior ou a mesma concentração de Cu2+ livre em solução? Justifique.
c) Uma forma de quantificar os íons Cu2+ na solução remanescente é por meio de titulação utilizando um agente complexante como o EDTA, que se liga ao Cu2+ formando um complexo estável de coloração azul. Sabendo que o ponto final da titulação de 10 mL da solução remanescente ocorre quando 25 mL de EDTA 0,01 mol/L são utilizados para complexar o Cu2+, calcule a concentração de Cu2+, em mol/L, nessa solução, considerando que a estequiometria do Cu2+ com EDTA é de 1:1, ou seja, na viragem, o número de mols de EDTA e de Cu2+ são iguais.
Gabarito:
Resolução:
a) A relação entre a concentração da proteína e o volume de água no sistema é inversamente proporcional, o que significa que à medida que a concentração da proteína diminui, o volume de água no sistema aumenta.
b) Maior, como a quantidade de proteína presente nesse mesmo volume é menor por causa da diluição, uma menor quantidade de cobre será utilizda para precitar, logo, sobrará mais íons Cu2+ na fase aquosa.
c) Como a proporção estequiométrica é 1:1, é possível calcular utilizando a fórmula CV=CV
Logo, ,
Dessa forma,