Questão 2
(IME - 2007/2008) Para cada molécula abaixo:
1) BeH2
2) BCl3
3) ácido fluorídrico
4) H2S
5) pentacloreto de antimônio
a) desenhe a fórmula estrutural, indicando a direção e o sentido dos vetores momento dipolar correspondentes a cada ligação química; e
b) responda se a molécula é polar ou apolar, justificando.
Gabarito:
Resolução:
a)
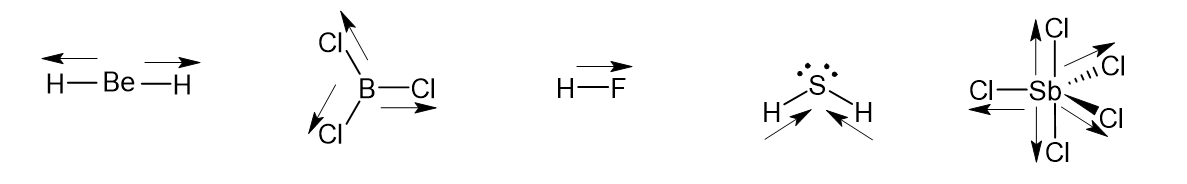
b)
1) BeH2: apolar. Como os átomos de hidrogênio atraem os elétrons da ligação Be-H para mais próximo dei com as mesmas intensidades e sentidos contrários, o vetor momento de dipolo resultante é nulo.
2) BCl3: apolar. A soma dos vetores momento de dipolo de cada ligação B-Cl é igual a zero.
3) ácido fluorídrico: polar. A molécula é formada por uma ligação entre dois átomos diferentes. Como os átomos são diferentes, há uma diferença de eletronegatividade entre os eles e, portanto, a ligação é polar.
4) H2S: polar. Como o ângulo de ligação é diferente de 180º, a soma dos vetores momento de dipolo é diferente de zero.
5) pentacloreto de antimônio: apolar. A soma dos vetores momento de dipolo no plano axial é zero, assim como a soma dos vetores momento de dipolo no plano equatorial.