Questão 4
(IME - 2007/2008)
Considere o polímero bio-absorvível obtido pela reação de polimerização do monômero a seguir:
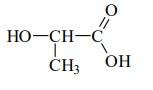
Prepara-se uma solução diluída com 30,60 g deste polímero em 2000 g de tetrahidrofurano (THF). O gráfico abaixo apresenta os diagramas de fase (sólido-líquido-vapor) desta solução diluída e de THF puro.
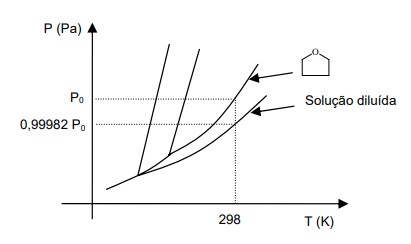
A partir dessas informações, determine:
a) o efeito coligativo numericamente evidenciado pelo gráfico;
b) a função orgânica formada na reação de polimerização;
c) a fórmula estrutural plana do mero (unidade repetitiva do polímero);
d) a massa molar média deste polímero na solução especificada; e
e) quantos gramas de água serão gerados na produção de 1 mol do polímero.
Gabarito:
Resolução:
a) O gráfico representa valores diferentes de pressões de vapor para o solvente puro e para a solução. A propriedade coligativa associada a essa representação é o abaixamento da pressão de vapor ou tonoscopia.
b) O produto formado na reação de polimerização é pertencente à função éster, que é formado pela reação entre o grupo carboxila e o grupo hidroxi do monômero.
c)
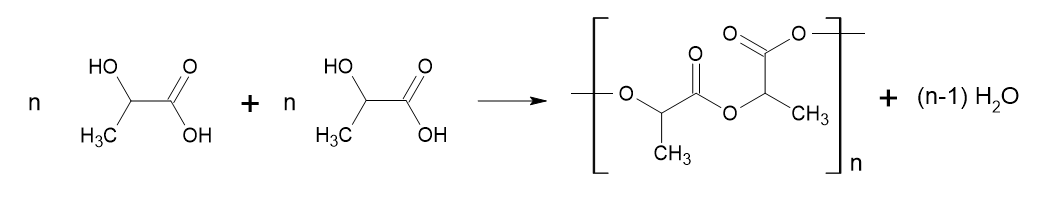
Portanto, a unidade repetitiva é representada por
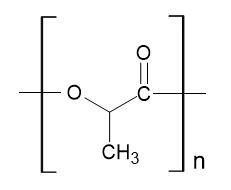
d) a massa molar média deste polímero na solução especificada; e
A fraçao molar de uma espécie é definida como a razão entre a quantidade de matéria dessa espécie e a quantidade de matéria total:
A massa molar é definida como a razão entre a massa e a quantidade de matéria:
e pode-se calcular a quantidade de matéria pela equação
Substituição na expressão da fração molar:
Nessa expressão, 1 representa o soluto e 2 representa o solvente. As massas do soluto (polímero e do solvente (THF) na solução foram fornecidas; a massa molar do THF é 72 gmol-1. Substituição dos valores:
e) quantos gramas de água serão gerados na produção de 1 mol do polímero.
O número de monômeros no polímero pode ser calculado pela razão entre a massa molar média do polímero e a massa molar do monômero:
A parir da equação da reação representada em c, observa-se que o número de moléculas de água formadas na reação de polimerização é N-1. Portanto, a quantidade de matéria de água formada na produção de 1 mol do polímero é 84 mol.
Cálculo da massa correspondente a 84 mol de H2O: