Questão 9
(IME - 2007/2008) A combustão completa de 3,0 g de um certo composto orgânico X produz, exclusivamente, 6,6 g de CO2 e 3,6 g de H2O. A 100 o C, 5,3 g de X (que se encontra no estado gasoso a esta temperatura) são misturados com 14 g de N2 em um recipiente de volume 3,0 litros. A pressão medida no interior do recipiente, nestas condições, é igual a 6,0 atm. Considere que os gases, no interior do recipiente, se comportam idealmente.
Sabendo que a reação de X com dicromato de potássio em ácido sulfúrico aquoso gera uma cetona, determine a composição centesimal do composto X, suas fórmulas mínima, molecular e estrutural, e dê a sua nomenclatura IUPAC.
Gabarito:
Resolução:
O composto X deve ter fórmula geral CaHb que tem uma reação geral de combustão:
CaHb + nO2 → aCO2 + b/2H2O
Sabemos que foi formado 6,6g de CO2:
a = 0,15
C0,15Hb + nO2 → 0,15CO2 + b/2H2O
Sabemos que foi formado 3,6g de H2O:
b/2 = 0,2 ⇒ b = 0,4
C0,15H0,40 + nO2 → 0,15CO2 + 0,20 H2O
A massa dessa quantidade encontrada para o composto X é:
A amostra tinha 3,0 g então podemos concluir que os 0,80 g que faltam são correspondentes a oxigênios presentes no composto X:
C0,15H0,40O0,05 + nO2 → 0,15CO2 + 0,20 H2O
C0,15H0,40O0,05 dividindo todos os índices para encontrar a fórmula mínima:
Fórmula mínima: C3H8O
Para encontrar a fórmula molecular vamos calcular a quantidade de mols de gás presente na amostra:
A quantidade de gás é a quantidade de X e a quantidade de N2 então:
Calculando a massa molar dessa quantidade de mols em 5,3g:
Massa molar que bate com a massa da fórmula mínima, com isso concluímos que a fórmula mínima é a fórmula molecular.
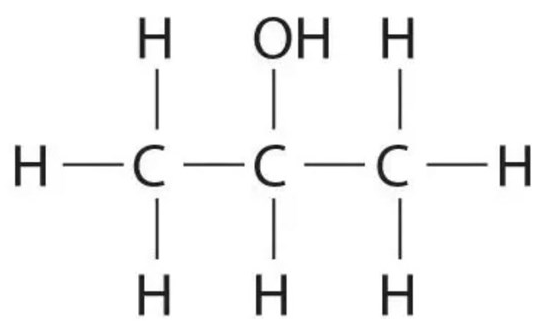
Pelo enunciado sabemos que a oxidação desse composto forma uma cetona, podemos concluir então que se trata de um álcool secundário:
propan-2-ol: