Questão 5
(IME - 2008/2009) A um reator de 16 L de capacidade, contendo 1 L de um líquido não-volátil e uma certa quantidade de um gás inerte não-solúvel, são adicionados dois gases puros e insolúveis A e B, que reagem entre si segundo a reação irreversível
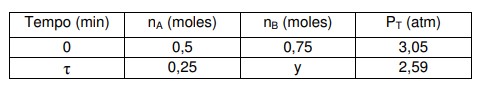
Considerando que o reator é mantido a 300 K durante a reação, que no instante inicial não há composto C no reator e utilizando os dados da tabela abaixo, determine a pressão total no reator ao término da reação.
Gabarito:
Resolução:
Calculando a quantidade inicial de mols:
A quantidade de gás inerte é então:
| A + | B + | inerte | → C | |
| inicio | 0,50 | 0,75 | 0,61 | - |
| reage | -0,50 | -0,50 | - | +0,50 |
| final | - | 0,25 | 0,61 | 0,50 |
Número final de mols é de 0,25 + 0,61 + 0,50 = 1,36 mol
Pelo cálculo da quantidade de mols no tempo τ existe uma diferença de 0,03 mol, como A , B e o gás inerte são insolúveis essa diferença corresponde à fração do gás C dissolvido no liquido. Podemos concluir então que a quantidade de C na fase gasosa é igual a 0,22 mols (0,25 - 0,03) e com isso para 0,50 mols será 0,44 mol. Fazendo com que a quantidade de gases seja: 0,25 + 0,61 + 0,44 = 1,30
A pressão final pode ser dada por: