Questão 8
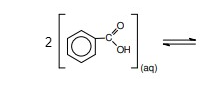
(IME - 2008/2009) Considere 100 mL de uma solução tampão aquosa (pH = 4,70) que contém 12,2 g de ácido benzóico (Ka=4,50 x 10-5). A fim de extrair o ácido dessa solução, utiliza-se o mesmo volume de um solvente orgânico imiscível em água. A mistura é agitada, deixada em repouso e, após a separação de fases, atinge o equilíbrio (Ke = 0,5):
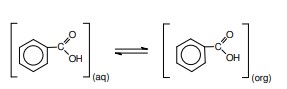
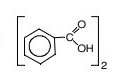
Na fase orgânica, o ácido benzoico não se dissocia, mas sofre o seguinte processo de dimerização parcial (Kd = 2):
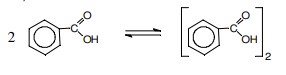
Calcule a concentração final do ácido benzoico na fase aquosa após a extração descrita acima.
Gabarito:
Resolução:
Calculando a massa molar do ácido benzoico:
Calculando a quantidade de mols de ácido benzoico:
Calculando a concentração inicial de ácido benzoico:
A concentração após adicionar 100 mL de solvente orgânico:
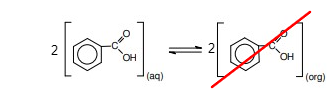
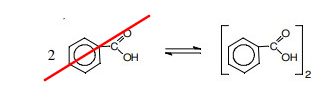
_____________________________________________

Não pode ser x'' pois daria um valor negativo, então a resposta é 0,3662 mol/L