Questão 31
(IME - 2009/2010) Considere as seguintes possibilidades para a estrutura da molécula de trifluoreto de cloro (ClF3):
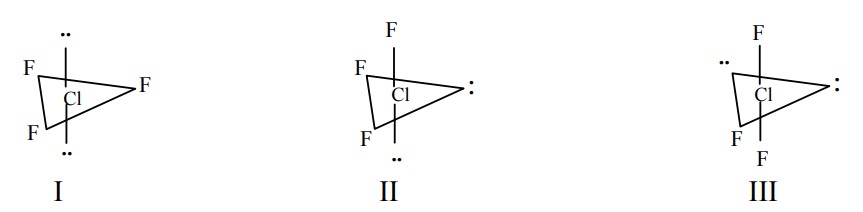
Assinale a alternativa correta.
A estrutura I é a mais estável, visto que as seis repulsões entre pares não-ligantes e pares ligantes equivalem à menor repulsão possível.
A estrutura II é a mais estável, visto que ocorrem três repulsões entre elétrons nãoligantes e pares ligantes e mais uma repulsão entre pares de elétrons não-ligantes, o que confere uma maior estabilidade ao sistema de forças.
A estrutura III é a mais estável por equivaler à configuração na qual a repulsão entre todos os pares (ligantes e não-ligantes) é mínima.
A estrutura I é a mais provável por ser a mais simétrica, correspondendo à configuração de menor energia.
Todas as três estruturas possuem a mesma energia e são encontradas na natureza
Gabarito:
A estrutura III é a mais estável por equivaler à configuração na qual a repulsão entre todos os pares (ligantes e não-ligantes) é mínima.
Resolução:
Solução I:
a) A estrutura I é a mais estável, visto que as seis repulsões entre pares não ligantes e pares ligantes equivalem à menor repulsão possível.
-FALSO. Da teoria de repulsão dos pares de elétrons, temos que quando há 5 nuvens eletrónicas em torno do átomo central e 3 ligantes, a geometria mais estável da molécula será "forma de T". Então a estrutura III é a mais estável.
b)A estrutura II é a mais estável, visto que ocorrem três repulsões entre elétrons não ligantes e pares ligantes e mais uma repulsão entre pares de elétrons não ligantes, o que confere uma maior estabilidade ao sistema de forças.
-FALSO. A estrutura III é a mais estável.
c) A estrutura III é a mais estável por equivaler à configuração na qual a repulsão entre todos os pares (ligantes e não ligantes) é mínima.
-VERDADEIRO. Da teoria VSEPR vista nas aulas de geometria molecular, temos que a geometria "forma de T" é a mais estável quando temos 5 nuvens e 3 ligantes ao redor do átomo central, isso porque as repulsões entre pares de elétrons, par-átomo e átomo-átomo são as menores nessa estrutura.
d) A estrutura I é a mais provável por ser a mais simétrica, correspondendo à configuração de menor energia.
-FALSO. A estrutura mais estável e, portanto, de menor energia é a III.
e) Todas as três estruturas possuem a mesma energia e são encontradas na natureza.
-FALSO. A estrutura III é a de menor energia devido ao mínimo de repulsões (tensões) no interior da molécula.
Solução II:
Resposta Correta: C
A geometria das nuvens eletrônicas do composto III é do tipo bipirâmide de base triangular.
A geometria molecular do composto III é do tipo T, que é mais estável (apresenta afastamento máximo entre os ligantes), pois a repulsão entre todos os pares (ligantes e não ligantes) é mínima.