Questão 10
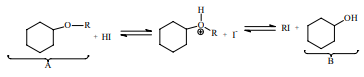
(IME - 2009/2010) A substância X, que pode ser obtida através da sequência de reações dada abaixo (onde R indica genericamente um grupo alquila), é constituída pelos elementos C, H e O.
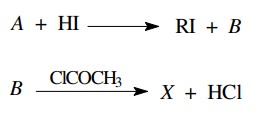
Uma amostra de 50,00 g de X sofre combustão completa, produzindo 123,94 g de CO2 e 44,37 g de H2O. Com base nas informações acima determine:
a) a fórmula mínima da substância X.
b) a fórmula molecular da substância X, sabendo-se que a sua massa molar é de 142,00 g/mol.
c) a fórmula estrutural plana da substância X, sabendo-se que, ao sofrer hidrólise ácida, esta molécula produz ácido acético e um álcool saturado que não possui átomos de carbono terciários ou quaternários.
d) a fórmula estrutural plana do composto B. e) a qual função orgânica pertence o reagente A.
Gabarito:
Resolução:
a) Uma amostra de 50,00 g de X sofre combustão completa, produzindo 123,94 g de CO2 e 44,37 g de H2O. Com base nas informações acima determine
Temos como fórmula genérica de combustão:
Foram produzidos 123,94g de CO2, que corresponde a:
Foram produzidos 44,37g de H2O, portanto:
Substituindo os valores encontrados na reação genérica:
Para calcular a quantidade de oxigênio no composto X, vamos então fazer o cálculo da massa de X com o que já encontramos de C e H:
Dividindo todos os valores por 0,7:
b) A massa molar da fórmula mínima é 71 g/mol, foi dito que a massa molar de X é de 142g/mol, ou seja, o dobro da massa molar da fórmula mínima. Dessa forma, multiplicamos todos os índices por 2:
c) É dito algumas informações no enunciado:
• Formação de ácido acético e um álcool saturado ... após sofrer hidrólise → éster
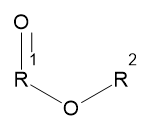
• O ácido formado é o ácido acético (ácido etanoico), portanto R1 tem 2 carbonos:
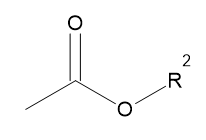
Já temos então, os 2 oxigênios da fórmula molecular, 2 dos 8 carbonos, então R2 tem 6 carbonos. Temos 5 dos 14 hidrogênios, faltam, portanto 9, com isso concluímos que a cadeia deve ser fechada (não pode ser insaturada, pois é dito que é saturada) para que a quantidade de hidrogênios fique correta. Chegamos então no seguinte desenho:
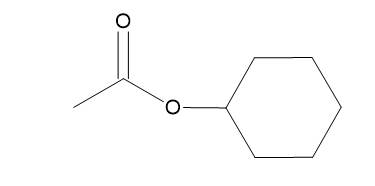
d) O composto (B) que reage com cloreto de ácido para formar X e eliminar HCl, é portanto:
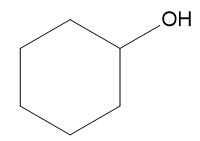
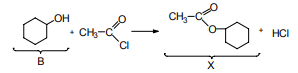
e)