Questão 9
[IME-2016/2017 - 2ª fase]
Um primeiro estudo da cinética da reação
SO2(g) + O3(g) → SO3(g) + O2(g)
foi feito a 250 K, fornecendo os dados da tabela abaixo:
| [SO2], mol/L | [O3], mol/L | Taxa, mol/(L.s) |
| 0,25 | 0,40 | 0,118 |
| 0,25 | 0,20 | 0,118 |
| 0,75 | 0,20 | 1,062 |
Um segundo estudo foi então realizado a 400 K, fornecendo:
| [SO2], mol/L | [O3], mol/L | Taxa, mol/(L.s) |
| 0,50 | 0,30 | 1,425 |
Com base nesses dados, estime a energia de ativação da referida reação.
Gabarito:
Resolução:
A partir dos dados da primeira tabela é possível identificar qual é a lei de velocidade para essa reação. Ao comparar o experimento 1 e 2, observa-se que ao dobrar a concentração de O3 a velocidade não se altera, portanto, a velocidade da reação tem ordem zero em relação a O3.
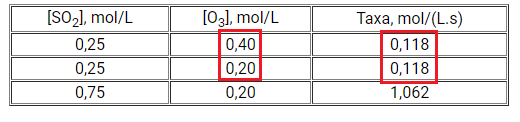
Já ao triplicar a concentração de SO2 do experimento 2 ao 3, a velocidade da reação é multiplicada por 9. Então, a lei de velocidade tem ordem 2 em relação ao SO2.
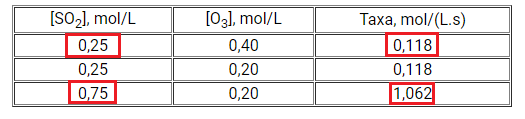
Unindo essas informações, encontra-se que a lei de velocidade é v = k·[SO2]2.
Utilizando os dados do primeiro experimento, é possível encontrar a constante de velocidade:
Partindo do princípio de que a lei de velocidade é a mesma na temperatura de 400 K, é possível encontrar a constante de velocidade nessa temperatura:
Sabendo o valor das duas constantes em diferentes temperaturas é possível, com a equação de Arrhenius, encontrar a energia de ativação:
Portanto a energia de ativação é de aproximadamente 6,097 kJ/mol.