Questão 8
(IME - 2023/2024)
Produz-se NH3(g) reagindo H2(g) com N2(g). A reação ocorre em uma temperatura T, 113 °C maior do que a temperatura em que a mesma deixa de ser espontânea.
Considere os dados termodinâmicos abaixo e que os mesmos não variam com a temperatura e com a pressão.
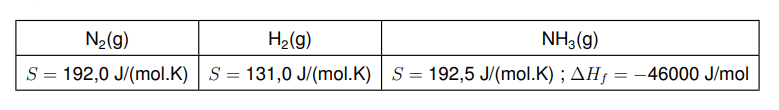
A partir dos dados do enunciado, pede-se:
a) calcular o valor de ;
b) determinar se a constante de equilíbrio da reação de produção da amônia é ,
ou
;
c) justificar em qual pressão, ou
, haverá maior produção de NH3(g) no equilíbrio.
Gabarito:
Resolução:
A reação balanceada é
Logo, é possível calcular a entropia da reação
Sendo assim, a temperatura onde ΔG=0
Logo,
b) Em T=573K, o ΔG>0, logo, verifica-se que K<1
c) Com o aumento de pressão, o equilíbrio se deslocará para a direita, segundo a Lei de Le Chatelier, sendo assim, a maior produção de amônia será em 200atm