Questão 10423
(ITA - 1993)
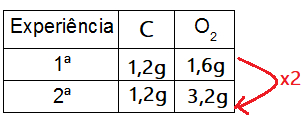
A observação experimental de que 1,20 g de carbono podem se combinar tanto com 1,60 g de oxigênio como com 3,20 g de oxigênio corresponde a uma confirmação da:
Lei de conservação das massas de Lavoisier.
Lei de Guldberg e Waage.
Regra de Proust, sobre pesos atômicos.
Lei das proporções múltiplas de Dalton.
Lei das proporções recíprocas de Richter e Wenzel.
Gabarito:
Lei das proporções múltiplas de Dalton.
Resolução:
Esses dados apresentados no exercícios fazem relação a lei das proporções múltiplas de Dalton. Essa lei diz que, ao fixar a massa de um dos elementos do composto, a proporção de outro elemento pode formar mais de uma substância variando em números inteiros.
Nesse caso, o carbono com massa fixa de 1,2 gramas pode combinar com o oxigênio de massa 1,6 gramas (CO) ou 3,2 gramas (CO2).