Questão 64604
(ITA) Um copo contém, inicialmente, 20mL de uma solução aquosa 0,1 molar de uma substância desconhecida. De uma bureta se deixa cair, gota a gota, uma solução aquosa 0,1 molar de outra substância, também desconhecida. Sabe-se que uma das substâncias em questão é um ácido e a outra uma base. Após a adição de cada gota da bureta, o pH do conteúdo do copo é monitorado e o resultado desta monitoração do pH é mostrado no gráfico a seguir
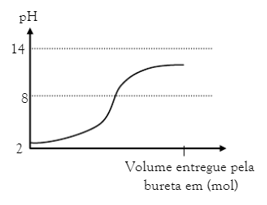
Da observação do gráfico acima, qual era a natureza das soluções iniciais no copo e na bureta? Respectivamente a Substância no copo e a Substância na bureta respectivamente:
ácido forte; base forte
base forte; ácido fraco
ácido fraco; base forte
ácido forte; base fraca
base fraca; ácido fraco
Gabarito:
ácido fraco; base forte
Resolução:
Inicialmente, temos um pH menor que sete indicando que no copo havia um ácido.
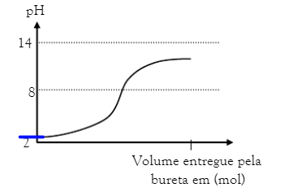
Como o pH da solução se torna alcalino (aumenta) isso indica que o conteúdo da bureta é uma base.
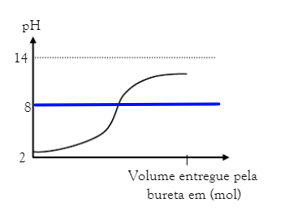
No ponto de equivalência, em destaque na imagem acima o pH é 8, pH > 7, uma solução alcalina, com isso podemos concluir que a base é mais forte que o ácido, portanto tínhamos um ácido fraco e uma base forte.