Questão 39904
(ITA 1997)
As notações e
serão utilizadas, respectivamente, para representar as variações de entalpia molar de dissolução e hidratação da espécie
em água.
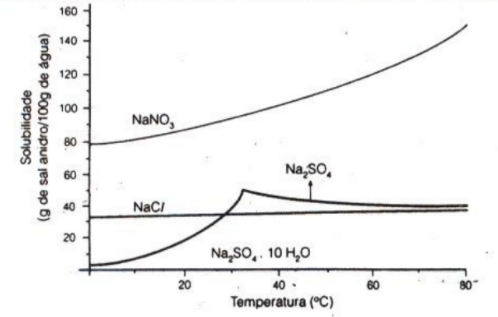
Considerando sistemas termodinamicamente estáveis, é errado afirmar que:
A 25°C, a solubilidade em água do NaNO3 é maior do que a do Na2SO4·10H2O.
A 25°C, uma mistura de 120 g de NaNO3 com 100 g de H2O é bifásica, sendo uma das fases o NaNO3 e a outra a H2O.
A 0°C, uma mistura de 20 g de NaCl com 100 g de água é monofásica, sendo esta fase uma solução aquosa não saturada em NaCl.
A 25°C, a concentração de íons de sódio existentes na fase líquida de uma mistura preparada pela adição de 6 g de NaCl à 100g de H2O é 1 mol/L.
A 25°C, a quantidade (mol) de íons de sódio presentes em uma solução preparada pela dissolução de 1,0 g de Na2SO4 em 10 g de H2O é maior do que a existente em outra solução preparada pela dissolução de 1,0 g de Na2SO4·10H2O na mesma quantidade de água.
Gabarito:
A 25°C, uma mistura de 120 g de NaNO3 com 100 g de H2O é bifásica, sendo uma das fases o NaNO3 e a outra a H2O.
Resolução:
Analisando cada uma das alternativas:
[A] Correta. É possível analisar no gráfico abaixo que a solubilidade do NaNO3 é maior que a do Na2SO4.
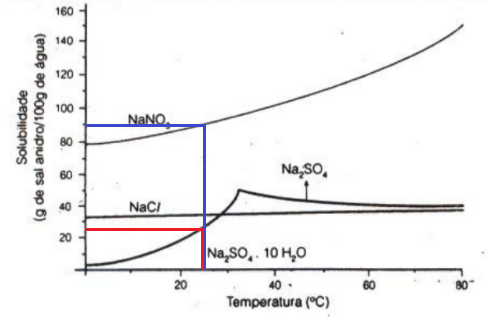
[B] Incorreta. Na temperatura de 25ºC, a solução é bifásica sendo uma fase de NaNO3 no corpo de fundo e a outra de uma solução saturada de NaNO3 em água.
[C] Correta. Na temperatura de 0ºC são solúveis em 100 g de água uma massa de aproximadamente 115 g de NaCl, então, uma mistura com 20 g de NaCl será monofásica e classificada como não saturada.
[D] Correta. A quantidade de matéria de Na proveniente de 6 g de NaCl é:
1 mol de NaCl --- 58,5 g --------- 23 g de Na+
6,0 g --------- x
x = 2,35 g de Na+
Como a massa molar do Na+ é 23g:
1 mol de Na+ ------ 23 g
y --------------------- 2,35 g
y = 0,1 mol de Na+
Essa quantidade de matéria está presente em 100 mL de água, então em 1000 mL:
0,1 mol de Na+ ------- 100 mL de água
z -------------------------- 1000 mL de água
z = 1 mol/L
Então, a concentração de Na+ é 1mol/L.
[E] Correta. A quantidade de íons sódio em cada um desses sais é:
1 mol de Na2SO4 ------ 142 g ---- 2 mol de Na+
1g ------ x
x = 1,39x10-2 mol de Na
1 mol de Na2SO4·10H2O ------ 322 g ------- 2 mol de Na+
1 g ------- y
y = 6,2x10-3 mol de Na+
Então, a quantidade de matéria de Na+ é maior em 1 g de Na2SO4 do que em 1 g de Na2SO4·10H2O.
Como a questão pede a alternativa incorreta, o gabarito é letra B.