Questão 29
(ITA - 2005)
Considere a curva de titulação a seguir, de um ácido fraco com uma base forte.
a) Qual o valor do pH no ponto de equivalência?
b) Em qual(ais) intervalo(s) de volume de base adicionado o sistema se comporta como tampão?
c) Em qual valor de volume de base adicionado pH = pKa?
Gabarito:
Resolução:
a) O ponto de equivalência é caracterizado pela igual concentração de H+ e OH-. No gráfico, o ponto de equivalência é representado pela inflexão assinalada a seguir:
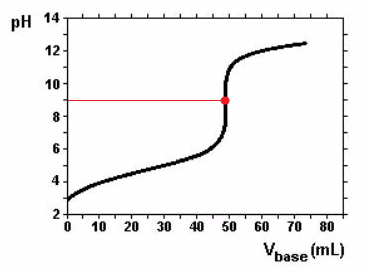
Sendo assim, o pH do ponto de equivalência é 9.
b) Uma solução tampão é caracterizada pela pequena variação de pH com a adição de base ou ácido. Graficamente é possível observar que a variação do pH é pequena entre 20 e 35 mL de base:
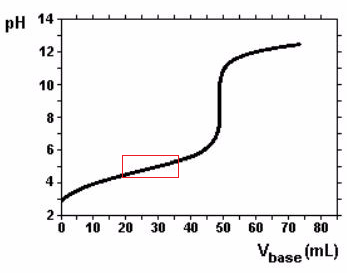
c) Partindo da equação:
Pode-se afirmar que pH será igual a pKa quando [A-] for igual a [HA]. A concentração de A- é igual à de HA no ponto de semiequivalência, ou seja, na metade do volume do ponto de equivalência. Sendo assim, pH é igual a pKa quando o volume de base é 25 mL.