Questão 10623
(ITA-2006/Adaptada)
Considere as seguintes espécies no estado gasoso: BF3, SnF3- , BrF3, KrF4 e BrF5. Para cada uma delas, qual é a hibridização do átomo central, respectivamente?
Gabarito:
sp2, sp3, dsp3, d2sp3, d2sp3
Resolução:
Cada ligação sigma e par de elétrons livres contribui 1 para a hibridação
sp3d2 ⇒ s p p p d d
1 ligação sigma ⇒
2 ligações sigma ⇒ sp
3 ligações sigma ⇒ sp2
4 ligações sigma ⇒ sp3
5 ligações sigma ⇒ sp3d
6 ligações sigma ⇒ sp3d2
BF3
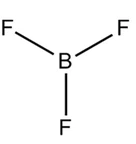
Átomo Central: B
3 ligações sigma: s p p = sp2
SnF3-
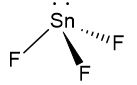
Átomo Central: Sn
3 ligações sigma + 1 par de elétrons livres: s p p p = sp3
BrF3
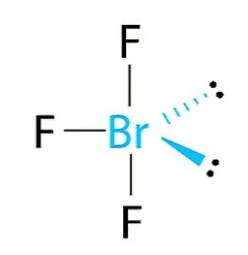
Átomo central: Br
3 ligações sigma + 2 pares de elétrons livres: s p p p d = sp3d
KrF4
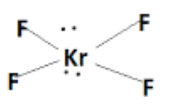
Átomo Central: Kr
4 ligações sigma + 2 pares de elétrons livres: s p p p d d = sp3d2
BrF5
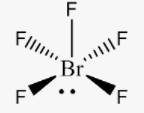
Átomo Central: Br
5 ligações sigma + 1 par de elétrons livres: s p p p d d = sp3d2
em ordem: sp2, sp3, dsp3, d2sp3, d2sp3