Questão 27
(ITA - 2006)
A equação química hipotética A → D ocorre por um mecanismo que envolve as três reações unimoleculares abaixo (I, II e III). Nestas reações, ΔHI representa as variações de entalpia, e EaI, as energias de ativação.
I. A → B; rápida, ΔHl, EaI
II. B → C; lenta, ΔHII, EaII
III. C → D; rápida, ΔHIII, EaIII
Trace a curva referente à energia potencial em função do caminho da reação A → D, admitindo que a reação global A → D seja exotérmica e considerando que: ΔHII > ΔHI > 0 ; EaI < EaIII.
Gabarito:
Resolução:
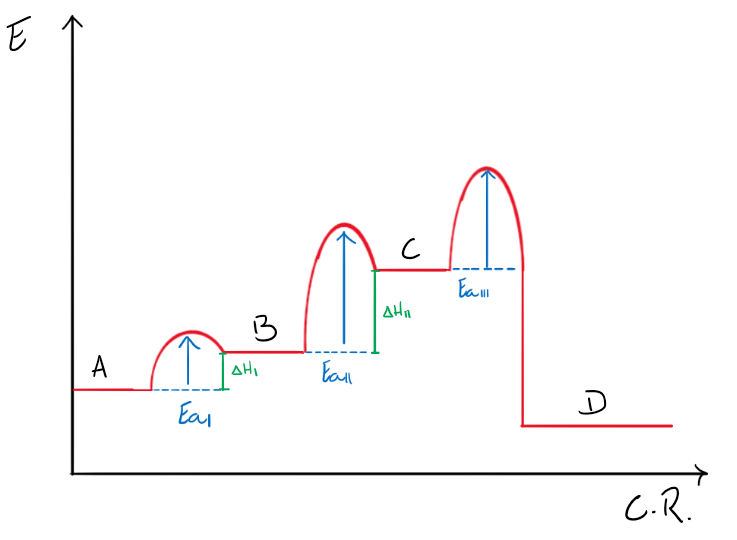
O eixo Y representa a energia e o eixo X o caminho da reação.
O gráfico acima cumpre os requisitos
1) ΔHI < ΔHII e
2) EaI < EaIII.
3) A energia de D é menor do que de A e, portanto, a reação A → D é exotérmica (ΔHr < 0).
Como a etapa 2 é a etapa lenta, EaII é maior que EaI e EaIII, mas EaIII continua sendo maior que EaI.