Questão 22
(ITA - 2009 - 2ª fase)
São fornecidas as seguintes informações relativas aos cinco compostos amínicos: A, B, C, D e E. Os compostos A e B são muito solúveis em água, enquanto que os compostos C, D, e E são pouco solúveis. Os valores das constantes de basicidade dos compostos A, B, C, D e E são, respectivamente, 1,0 × 10-3; 4,5 × 10-4; 2,6 x 10-10; 3,0 × 10-12 e 6,0 × 10-15. Atribua corretamente os dados experimentais apresentados aos seguintes compostos: 2-nitroanilina, 2-metilanilina, 2-bromoanilina, metilamina e dietilamina. Justifique a sua resposta.
Gabarito:
Resolução:
Estruturas dos compostos da questão:
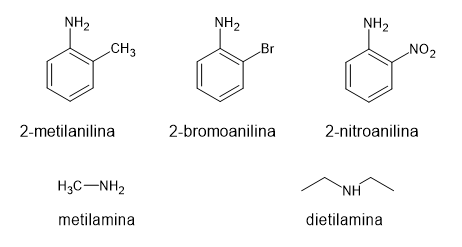
Relação entre as constantes de basicidade:
A: 1,0 × 10-3
B: 4,5 × 10-4
C: 2,6 x 10-10
D: 3,0 × 10-12
E: 6,0 × 10-15
Dos cinco compostos apresentados, três são aromáticos e dois são alifáticos. Em geral, compostos alifáticos possuem maior caráter básico do que compostos aromáticos porque o par de elétrons do nitrogênio em compostos aromáticos faz parte do sistema pi do anel e, portanto, o composto possui estabilização via ressonância. Como as constantes de basicidade de A e B são maiores do que as de C, D e E, as aminas A e B são alifáticas e as aminas C, D e E são aromáticas.
Também é possível fazer essa distinção entre os compostos analisando a solubilidade. Dos compostos citados, os aromáticos são pouco solúveis em água e os alifáticos são solúveis em água.
A dietilamina é mais básica do que a metilamina por possuir dois grupos doadores de elétrons ligados ao nitrogênio, fazendo com que o par de elétrons do nitrogênio esteja mais disponível para reagir como base em reações ácido-base. Portanto, o composto A é a dietilamina e o composto B é a metilamina.
Comparando os compostos C, D e E, todos possuem um grupo ligado ao anel na posição orto em relação ao grupo amino. O -Br e o -NO2 são grupos retiradores de elétrons e o -CH3 é grupo doador de elétrons. O efeito retirador de elétrons do grupo nitro é mais forte do que o do -Br. Analogamente ao raciocínio anterior, o grupo doador de elétrons faz com que o par de elétrons do grupo amino esteja mais disponível para reagir como base. Portanto, a 2-metilanilina é mais básica que a 2-bromoanilina que é mais básica 2-nitroanilina.
A: 1,0 × 10-3 ⇒ dietilamina
B: 4,5 × 10-4 ⇒ metilamina
C: 2,6 x 10-10 ⇒ 2-metilanilina
D: 3,0 × 10-12 ⇒ 2-bromoanilina
E: 6,0 × 10-15 ⇒ 2-nitroanilina