Questão 70732
(ITA - 2017)
Num experimento que mede o espectro de emissão do átomo de hidrogênio, a radiação eletromagnética emitida pelo gás hidrogênio é colimada por uma fenda, passando a seguir por uma rede de difração. O espectro obtido é registrado em chapa fotográfica, cuja parte visível é mostrada na figura.

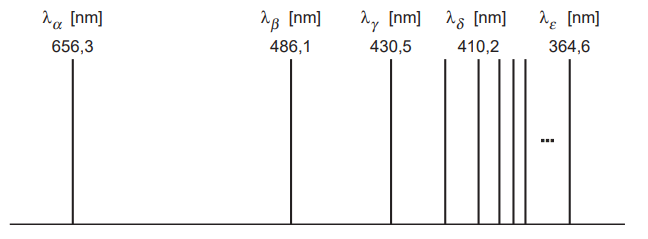
Pode-se afirmar que
O modelo de Bohr explica satisfatoriamente as linhas do espectro visível do átomo de Hidrogênio.
Da esquerda para a direita as linhas correspondem a comprimentos de onda do violeta ao vermelho.
O espaçamento entre as linhas adjacentes decresce para um limite próximo ao infravermelho.
As linhas do espectro encontrado são explicadas pelo modelo de Rutherford.
Balmer obteve em 1885 a fórmula empírica para o comprimento de onda em que n = 3, 4 ... e R é a constante de Rydberg.
Gabarito:
O modelo de Bohr explica satisfatoriamente as linhas do espectro visível do átomo de Hidrogênio.
Resolução:
Analisando as alternativas:
A) [CORRETA] No modelo de Bohr, os elétrons orbitam ao redor do núcleo em órbitas circulares em níveis de energia quantizadas. Quando o elétron absorve energia, ele salta de uma órbita mais interna para outra mais externa, já quando ele emite energia, ele salta de uma órbita mais externa para outra mais interna, sendo que essa emissão e absorção se dá de modo quantizado. Esse processo explica satisfatoriamente as linhas do espectro visível do átomo de hidrogênio.
B) [INCORRETA] O comprimento de onda correspondente ao vermelho está entre, aproximadamente, 625 nm à 740 nm, e o correspondente ao violeta é de, aproximadamente, 380 nm à 440 nm. Logo, da esquerda para a direita as linhas correspondem a comprimentos de onda do vermelho ao violeta, não ao contrário.
C) [INCORRETA] O infravermelho corresponde a frequências menores, logo, comprimentos de onda maiores que do vermelho:
Assim, observando o espectro da direita para a esquerda, pode-se perceber que o espaçamento entre as linhas adjacentes crescem para um limite próximo ao infravermelho (λ > 740 nm).
D) [INCORRETA] Como Rutherford não relaciona a emissão às trocas de níveis de energia, nem aborda a quantização de energia, ele não explica as linhas do espectro satisfatoriamente.
E) [INCORRETA] A fórmula correta obtida por Balmer é:
