Questão 5
(ITA - 2024)
Os dados da tabela abaixo foram obtidos em um estudo de determinação dos parâmetros cinéticos de uma reação hipotética e irreversível do tipo A + B → C + D.
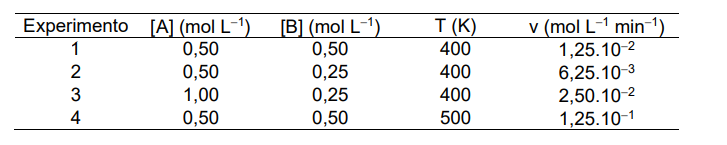
Não havendo mudança no mecanismo da reação no intervalo de temperatura considerado, determine os seguintes valores numéricos:
a) Ordem da reação em relação ao reagente A.
b) Ordem da reação em relação ao reagente B.
c) Ordem global da reação.
d) Constante de velocidade da reação a 400 K, com sua respectiva unidade de medida.
e) Constante de velocidade da reação a 500 K, com sua respectiva unidade de medida.
f) Energia de ativação da reação, em kcal mol-1.
Gabarito:
Resolução:
a) Ordem da reação em relação ao reagente A.
Utilizando o experimento 2 e 3,
Reação de segunda ordem em relação ao reagente A
b) Ordem da reação em relação ao reagente B.
Utilizando os experimentos 1 e 2,
Reação de primeira ordem em relação ao reagente B.
c) Ordem global da reação.
Como, v=k[A]2[B]1, é possível concluir que a orgem global da reação é 3.
d) Constante de velocidade da reação a 400 K, com sua respectiva unidade de medida.
Utilizando o experimento 1,
Como,
, então,
e) Constante de velocidade da reação a 500 K, com sua respectiva unidade de medida.
De forma análoga à alternativa d, encontramos:
f) Energia de ativação da reação, em kcal mol-1.
Utilizando a equação de Arrhenius,
Substituindo os valores encontrados anteriormente é obtido