Questão 30108
MACKENZIE 2005
Química
(Mack-2005) Dadas as energias de ligação em kJ/mol (valores absolutos), o calor, em kJ/mol, da reação abaixo equacionada é
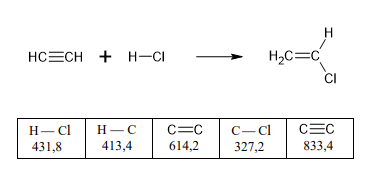
A
+323,8.
B
–431,8.
C
–521,4.
D
–89,6.
E
+104,6.
Gabarito:
–89,6.
Resolução:
A variação de entalpia de uma reação, usando energias de ligação, é igual à soma das energias das ligações quebradas menos a soma das energias das ligações formadas.
Assim, tomando a equação dada no enunciado, temos que:
H =
Hquebradas -
Hformadas = (HC≡C + 2*HH-C + HH-Cl) - (3*HH-C + HC-Cl + HC=C) = (833,4 + 2*413,4 + 431,8) kJ/mol - (3*413,4 + 327,2 + 614,2) kJ/mol =
= -89,6 kJ/mol