Questão 19363
(PUC-PR 2016)
“O ácido sulfúrico é tido como um indicador da economia de um país, pois é o produto químico mais utilizado pela indústria. Sua aplicação tem larga escala, desde em fertilizantes e baterias de automóveis, até no refino do petróleo. É extremamente solúvel em água, porém, isto deve ser feito com muita cautela, pois seus vapores são liberados agressivamente”.
Disponível em: http://www.brasilescola.com/
Uma das maneiras de produzi-lo é através das reações com oxigênio, o qual ocupa uma fração de 21%, aproximadamente, no ar atmosférico. A partir das informações fornecidas e utilizando as reações não balanceadas apresentadas a seguir, referentes às etapas de produção de ácido sulfúrico.
Dados:
(Ma(g/mol): H = 1,O = 16, S = 32).
Volume molar na CNTP: 22,71 L/mol.
Avogadro = 6 x 1023.
I. S8(s) + O2(g) → SO2(g)
II. SO2(g) + O2(g) → SO3(g)
III. SO3(g) + H2O(l) → H2SO4(aq)
Assinale a alternativa CORRETA.
Para produzir 40 g de ácido sulfúrico, são necessárias 17 g de enxofre.
Devemos colocar cuidadosamente a água no ácido, pois seus vapores são liberados, podendo causar queimaduras graves no corpo do manuseador.
O volume de ar que conterá O2(g) suficiente para combustão completa de 50 g de enxofre será de aproximadamente 253 L.
O ácido sulfúrico também pode ser denominado anidrido sulfuroso.
Para se obter 1,2×1021 moléculas de ácido sulfúrico, há necessidade de 3×10-4 mol de dióxido de enxofre.
Gabarito:
O volume de ar que conterá O2(g) suficiente para combustão completa de 50 g de enxofre será de aproximadamente 253 L.
Resolução:
Analisando cada uma das alternativas:
[A] Incorreta. Essa é uma reação que ocorre em etapas, portanto, a equação global é obtida somando as três:
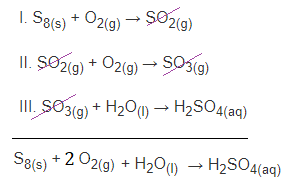
Portanto, a equação global balanceada é:
1 S8(s) + 12 O2(g) + 8 H2O(l) → 8 H2SO4(aq)
A proporção de enxofre e ácido sulfúrico é 1 mol S8 : 8 mol H2SO4. Como a alternativa trabalha com os dados em massa, é preciso transformar quantidade de matéria em massa, e pra isso usamos a massa molar. A massa molar do S8 é 256g/mol e do H2SO4 é 98g/mol, então a proporção em massa é:
1 mol S8 : 8 mol H2SO4.
256 g S8 : 784 g H2SO4.
Para se obter 40 g de ácido sulfúrico a massa necessária de enxofre será:
256 g S8 --------- 784 g H2SO4.
x --------------------- 40 g de H2SO4
x = 13,06 g de S8.
Portanto, a massa necessária de enxofre é 13,06g e não 17g.
[B] Incorreta. Devemos verter sempre o ácido na água porque a diluição é exotérmica, portanto, a temperatura se eleva muito. Ao verter o ácido na água, caso haja algum tipo de "espirramento", vai ser água e não ácido.
[C] Correta. A proporção do enxofre para o oxigênio é 1 mol S8(s) :12 mol O2(g). Portanto, a proporção em massa de enxofre e quantidade de matéria de O2 vai ser:
1 mol S8(s) :12 mol O2(g)
256g S8(s) :12 mol O2(g).
Para reagir com 50g de enxofre a quantidade de matéria de O2 necessária é:
256g S8(s) --------- 12 mol O2(g).
50g de S8 ------- x
x = 2,34 mol de O2
Parra converter a quantidade de matéria em volume, utiliza-se o dado de volume molar:
1 mol de O2 -------- 22,71 L
2,34 mol de O2 ----- x
x = 53,14 L de O2
O volume necessário de O2 é esse, porém, a questão pergunta a respeito do volume de ar. Como 21% do ar é composto por O2 é necessário encontrar o volume de ar no qual 53,14 L corresponde a 21%:
53,14 L ------------ 21%
x --------------------- 100%
x = 253 L de ar
[D] Incorreta. Anidrido sulfuroso é aquele obtido pela desidratação do H2SO3, portanto é o SO2.
[E] Incorreta. Como essa alternativa quer uma relação entre dióxido de enxofre e ácido sulfúrico, é necessário somar as equações II e III.
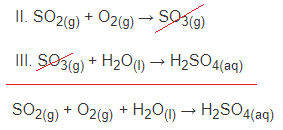
Portanto, a equação global balanceada é:
2 SO2(g) + O2(g) + 2 H2O(l) → 2 H2SO4(aq)
A constante de avogadro indica a quantidade de moléculas em 1 mol, portanto a proporção entre SO2 e H2SO4 em quantidade de moléculas é:
2 mol de SO2 : 2 mol de H2SO4
2 · 6x1023 : 2 · 6x1023
Então, a proporção é 1:1. Por isso, para obter 1,2x1021 moléculas de H2SO4 são necessárias 1,2x1021 moléculas de SO2.