Questão 46301
(CSA) Na figura abaixo está mostrado o gráfico pressão x volume para uma amostra de gás ideal, que sofre as transformações A → B → C → A. A transformação C → A é isotérmica.
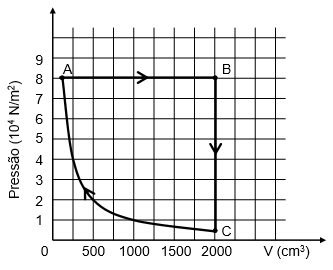
Sobre a mesma situação, é FALSO afirmar:
No processo C → A, há transferência de calor da amostra de gás para a vizinhança
No processo A → B → C, há um trabalho total positivo realizado pelo gás sobre a vizinhança
No processo completo A → B → C → A, há um trabalho total positivo realizado pelo gás sobre a vizinhança, mas seu valor é menor que 130 J.
No processo B → C, não há qualquer realização de trabalho, nem pela amostra de gás, nem pela vizinhança, e há transferência de calor da vizinhança para o sistema
Gabarito:
No processo B → C, não há qualquer realização de trabalho, nem pela amostra de gás, nem pela vizinhança, e há transferência de calor da vizinhança para o sistema
Resolução:
A transformação BC, como mostrada no diagrama, é uma isovolumétrica. Portanto, não há variação de volume, indicando que o gás não sofre nem realiza nenhum trabalho.
Mas o erro na alternativa está em dizer que o calor flui do ambiente para o sistema.
Pela primeira Lei Q = W + ΔU.
Nesse caso W = 0, então Q = ΔU, mas ΔU é negativo, pois a temperatura está diminuindo, então o calor está saindo do sistema.