Questão 25175
(UEFS 2017)
O ácido bórico, H3BO3, em baixas concentrações, é utilizado no tratamento de infecções do canal auditivo externo, inflamação nos olhos, irritação da pele, irritação dos olhos, picada de insetos e queimaduras leves. Entretanto, em algumas pessoas, o contato com o ácido bórico pode causar reações alérgicas, irritação nos olhos e do sistema respiratório. Em doses elevadas, o ácido bórico é frequentemente utilizado como inseticida para matar baratas, formigas, pulgas e muitos outros insetos.
Sobre o ácido bórico, é correto afirmar:
É um ácido fraco e pode ser preparado pela reação de B2O3 com água.
O átomo de boro, nesse composto, realiza seis ligações covalentes simples e possui geometria molecular igual a do SF6.
O átomo de boro, nesse composto, possui oito elétrons na camada de valência e, com isso, possui seu subnível de energia p preenchido com seis elétrons.
A reação de neutralização desse ácido com hidróxido de cálcio produz CaBO3 e água.
Nesse composto, o átomo de boro, por ser menos eletronegativo que o oxigênio, doa seus elétrons de valência aos átomos de oxigênio, atingindo assim uma configuração de gás nobre.
Gabarito:
É um ácido fraco e pode ser preparado pela reação de B2O3 com água.
Resolução:
a) Correto. É um ácido fraco e pode ser preparado pela reação de B2O3 com água.
nº de oxigênio - nº de hidrogênios ionizáveis = 3 - 3 = 0 → Ácido Fraco
B2O2 + 3H2O → 2H3BO3
b) Incorreto. O átomo de boro, nesse composto, realiza seis ligações covalentes simples e possui geometria molecular igual a do SF6.
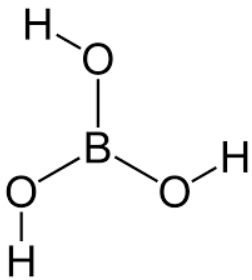
São 3 ligações covalentes que o boro faz.
c) Incorreto. O átomo de boro, nesse composto, possui oito elétrons na camada de valência e, com isso, possui seu subnível de energia p preenchido com seis elétrons.
Vendo a imagem no item B, podemos identificar que possui seis elétrons na camada de valência e não 8.
d) Incorreto. A reação de neutralização desse ácido com hidróxido de cálcio produz CaBO3 e água.
2 H3BO3 + 3 Ca(OH)2 → Ca(BO3)2 + 6 H2O
e) Incorreto. Nesse composto, o átomo de boro, por ser menos eletronegativo que o oxigênio, doa seus elétrons de valência aos átomos de oxigênio, atingindo assim uma configuração de gás nobre.
A ligação é covalente e não iônica, portanto não há doação de elétrons