Questão 10105
(UEL-PR) Potenciais-padrão de redução:
H+, ½ H2 .................. E = 0,00 volt
Cu2+, Cu ................... E = + 0,34 volt
Fe2+, Fe ..................... E = - 0,44 volt
Se em vez do par H+, ½ H2 , escolhido como tendo potencial-padrão de redução igual a zero, fosse escolhido o par Fe2+, Fe como padrão, fixando-se a este o valor zero, nessa nova escala, os potenciais-padrão de redução, dos pares Cu2+, Cu e H+, ½ H2 , seriam, respectivamente, em volt:
+0,10 e +0,34
-0,10 e -0,34
-0,78 e -0,44
-0,78 e +0,44
+0,78 e +0,44
Gabarito:
+0,78 e +0,44
Resolução:
Resolução 1
Os potencias de redução são dados em relação à um padrão, que naturalmente é o eletrodo de hidrogênio.
Isto significa que, sendo o potencial absoluto do eletrodo de hidrogênio igual a X, temos que o potencial dos demais são dados da seguinte forma:
ECu2+/Cu = ECu2+/Cu absoluto - X = +0,34 V
EFe2+/Fe = EFe2+/Fe absoluto - X = -0,44 V
EH+/H2 = X - X = 0 V
Sendo assim, tornando o eletrodo Fe2+/Fe como padrão, teremos o seguinte:
ECu2+/Cu = ECu2+/Cu absoluto - EFe2+/Fe absoluto (I)
EH+/H2 = X - EFe2+/Fe absoluto (II)
Contudo, sabemos que EFe2+/Fe absoluto = -0,44 V + X, então, substituindo em (I) e (II), temos:
ECu2+/Cu = ECu2+/Cu absoluto - (-0,44 V + X) = ECu2+/Cu absoluto - X + 0,44 = 0,34 + 0,44 = +0,78 V
EH+/H2 = X - EFe2+/Fe absoluto = X - (-0,44 V + X) = +0,44 V
Resolução 2
Analisando como uma reta numérica, é só fazer a migração dos valores considerando Fe+2/Fe como o ponto zero.
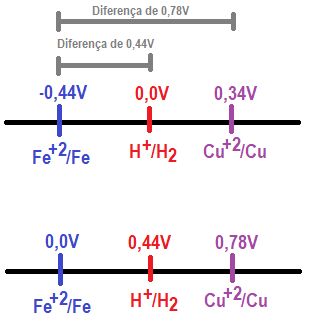
Gabarito: letra E