Questão 64239
(UEMG)
Ebulioscopia é a propriedade coligativa, relacionada ao aumento da temperatura de ebulição de um líquido, quando se acrescenta a ele um soluto não volátil.
Considere as três soluções aquosas a seguir:
Solução A = NaCl 0,1 mol/L
Solução B = sacarose 0,1 mol/L
Solução C = CaCl2 0,1 mol/L
As soluções foram colocadas em ordem crescente de temperatura de ebulição em
C, A, B.
B, A, C.
A, B, C.
C, B, A.
Gabarito:
B, A, C.
Resolução:
A adição de soluto não volátil leva ao aumento da temperatura de ebulição, provocado pela interação entre o soluto e o solvente. Portanto, quanto maior for o número de partículas em solução, maior o efeito do soluto e maior a temperatura de ebulição.
Por isso, é preciso analisar o número de partículas formadas por cada um desses solutos adicionados:
• NaCl
A dissociação do NaCl é representada pela equação NaCl → Na+ + Cl-, ou seja, é uma dissociação 1:1:1. Se foram adicionados 0,1 mol a quantidade de partículas ao final é:
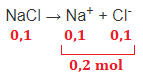
• Sacarose
A sacarose é um composto molecular, então não dissocia em água. Portanto, a quantidade de partículas é a mesma adicionada:
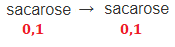
• CaCl2
A dissociação do CaCl2 é representada pela equação CaCl2 → Ca+2 + 2 Cl-, ou seja, é uma dissociação 1:1:2. Se foram adicionados 0,1 mol a quantidade de partículas ao final é:
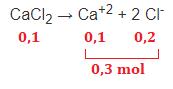
Então, a temperatura de ebulição é mais baixa quanto menor for o número de partículas, então:
TEsacarose < TENaCl < TECaCl2
Então, a solução B tem temperatura de ebulição menor que A, que é menor que C.
Gabarito: letra B