Questão 19283
(UERJ 2014)
O conjunto de elementos químicos englobados no grupo 3 e no bloco f da tabela de classificação periódica dos elementos, com exceção dos actinídeos, é denominado “metais terras raras”.
Esses metais são encontrados comumente na forma de óxidos, sendo o caráter iônico dos óxidos diretamente proporcional ao raio atômico do metal.
O metal terra rara componente do óxido de maior caráter iônico possui o seguinte símbolo:
Ac.
La.
Lu.
Sc.
Gabarito:
La.
Resolução:
Em geral, quanto maior a diferença de eletronegatividade entre os átomos, maior o caráter iônico da ligação. E a eletronegatividade é inversamente proporcional ao raio.
Então, como se tratam de óxidos, ou seja, compostos diatômicos com oxigênio, o oxigênio não vai ter seu raio ou eletronegatividade alterados, então, para que o caráter iônico aumente, a eletronegatividade do outro elemento precisa diminuir para aumentar a diferença, ou seja, o raio precisa aumentar.
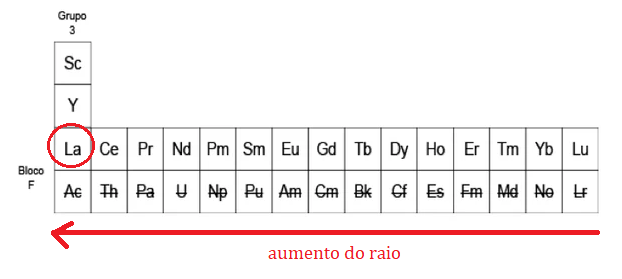
Sabendo que o raio atômico de um elemento nos grupos da tabela periódica aumenta de cima para baixo e nos períodos da direita para a esquerda, o metal "terras raras" com o maior raio entre as alternativas é o lantanídeo, de símbolo La.
Gabarito: letra B