Questão 9706
(UFES - 2004)
Um ácido carboxílico será tanto mais forte, quanto mais estável for sua base conjugada (carboxilato). A base conjugada é normalmente estabilizada pela presença de grupos retiradores de elétrons adjacentes à carbonila, que tendem a reduzir, por efeito indutivo, a densidade de carga sobre o grupo carboxilato.
Baseado nessas afirmações, assinale a alternativa que apresenta o ácido mais forte:
CH3COOH
CℓCH2COOH
CℓCH2CH2COOH
Cℓ2CHCOOH
HCOOH
Gabarito:
Cℓ2CHCOOH
Resolução:
Analisando cada estrutura:
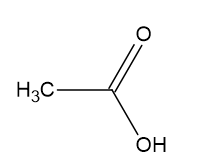
A) CH3COOH
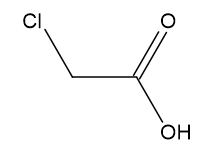
B) CℓCH2COOH
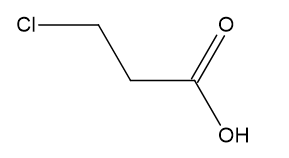
C) CℓCH2CH2COOH
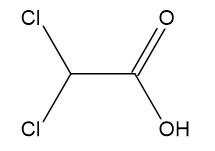
D) Cℓ2CHCOOH
E) HCOOH
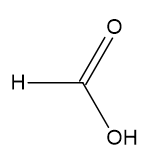
A força do ácido está ligada com os ligantes nele. Quanto mais eletronegativos esses ligantes, mais fraca será a ligação entre oxigênio e hidrogênio devido a baixa densidade eletrônica. Dessa forma, por ser mais fraca, o ácido vai liberar mais facilmente íons H+, sendo, então, um ácido mais forte. Dentre as opções, aquele que apresenta maior número de átomos muito eletronegativos é o Cℓ2CHCOOH.