Questão 9295
(UFRN 2004)
Um estudante recebeu uma tabela, reproduzida a seguir, em que constam algumas propriedades físicas de três compostos diferentes:
| Composto | Ponto de fusão (ºC) | Ponto de ebulição (ºC) | Solubilidade em água a 25 ºC |
| I | -138 | 0 | insolúvel |
| II | -90 | 117,7 | solúvel |
| III | -116 | 34,6 | parcialmente solúvel |
Segundo essa tabela, os possíveis compostos I, II e III são, respectivamente,
Gabarito:
n-butano, 1-butanol e éter etílico.
Resolução:
Quanto maior a interação molecular, maior tende a ser o ponto de ebulição, fusão e a solubilidade em água, por ser mais polar.
1ª Íon-Dipolo > 2ª Ligação de Hidrogênio > 3ª Dipolo-Dipolo > 4ª Van Der Walls (Dipolo Induzido - Dipolo Induzido)
Quem tem maior ponto de ebulição e solubilidade em água é o mais polar.
Quem tem menor ponto de ebulição e solubilidade em água é o menos polar.
éter etílico (III) intermediário
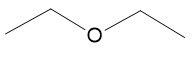
Há oxigênio, que é um polo, porém é um polo fraco, por não ter ligação de hidrogênio.
1-butanol (II) mais polar e solúvel
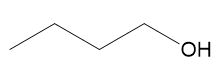
Possui ligação de hidrogênio, como tem apenas 4 carbonos na parte hidrofóbica, não impede tanto a solubilização do composto em água.
n-butano (I) menos polar e solúvel
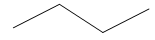
Todo o composto é hidrofóbico, todas as ligações são Van der Walls