Questão 18
A figura mostra a variação do raio atômico com o número atômico.
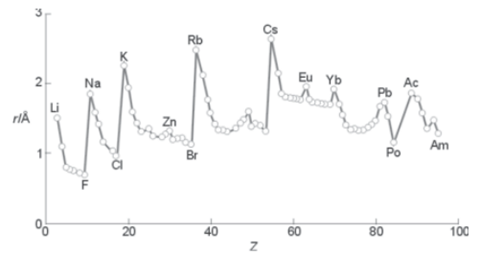
Figura: Variação do raio atômico ao longo da tabela periódica.
Tabela periódica e propriedades periódicas. Disponível em: https://cesad.ufs.br/ORBI/public/uploadCatalago/11365527032012Quimica_Inorganica_I_Aula_2.pdf. Acesso em: 19 fev. 2022. (Adaptado).
Com base nos elementos identificados na figura, é correto afirmar que os que apresentam maior energia de ionização são
Po, Zn e Am, por serem os metais que têm os menores raios atômicos.
F, Cl e Br, por serem os elementos que têm os menores raios atômicos.
K, Rb e Cs, por serem os elementos que apresentam os maiores raios atômicos.
Li, F e Na, por serem os elementos que possuem os menores números atômicos.
Po, Ac e Am, por serem os elementos que possuem os maiores números atômicos.
Gabarito:
F, Cl e Br, por serem os elementos que têm os menores raios atômicos.
Resolução:
A) Incorreto. Os elementos que possuem maior energia de ionização são aqueles que possuem o menor raio atômico. Os elementos citados são os metais com menor raio atômico, mas não são os elementos com menor raio atômico.
B) Correto. De acordo com os dados apresentados na figura, os elementos flúor (F), cloro (Cl) e bromo (Br) apresentam os menores raios atômicos. Como a energia de ionização (energia mínima necessária para retirar um elétron da camada de valência) e o raio atômico apresentam relação inversa, ou seja, quanto menor o raio atômico, maior a energia de ionização, esses elementos são os que apresentam maior energia de ionização entre os elementos identificados na figura.
C) Incorreto. Considera os elementos de maior raio atômico como aqueles que apresentam maior energia de ionização, quando na verdade são os que possuem menor raio atômico.
D) Incorreto. Considera que a energia de ionização é maior nos elementos de menor número atômico, encontrados mais à esquerda na figura, quando na verdade está associada ao raio atômico.
E) Incorreto. Considera que a energia de ionização é maior nos elementos de maior número atômico, encontrados mais à direita na figura, quando na verdade está associada ao raio atômico.