Questão 24796
(UFU 2014 - meio do ano) Ao se misturar 50 mL de água com 50 mL de álcool etílico, o volume final será 96 mL e não 100 mL, como era de se esperar.
Essa contração no volume pode ser explicada pela (s):
reação que ocorre entre a água e o álcool, gerando gases que são liberados da solução.
miscibilidade entre a água e o álcool, independentemente da proporção desses líquidos.
ligações de hidrogênio formadas entre as moléculas de água e as de álcool.
mistura azeotrópica que se forma entre a água e o álcool, cujo ponto de ebulição é constante.
Gabarito:
ligações de hidrogênio formadas entre as moléculas de água e as de álcool.
Resolução:
Analisando as alternativas:
A) reação que ocorre entre a água e o álcool, gerando gases que são liberados da solução.
INCORRETO. A reação entre a água e o álcool não vai gerar gases.
B) miscibilidade entre a água e o álcool, independentemente da proporção desses líquidos.
INCORRETO. A água e o álcool são líquidos miscíveis, mas isso não explica a diminuição do volume.
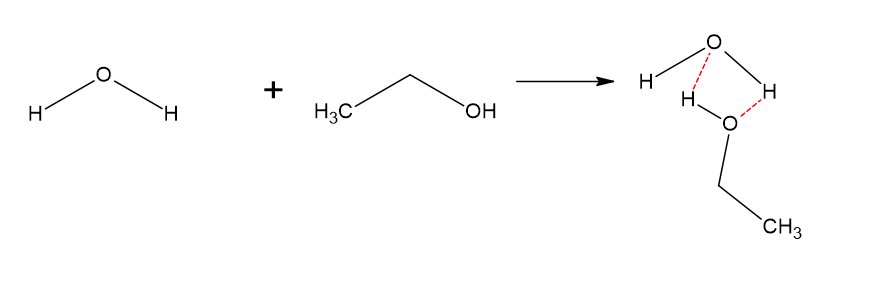
C) ligações de hidrogênio formadas entre as moléculas de água e as de álcool.
CORRETO. O álcool é solúvel na água, formando ligações de hidrogênio entre as moléculas das duas substâncias. O rearranjo dessas moléculas promove uma diminuição da distância entre elas, fazendo com que ocorra a diminuição do volume inicial de ambos os compostos.
D) mistura azeotrópica que se forma entre a água e o álcool, cujo ponto de ebulição é constante.
INCORRETO. A mistura entre água e o álcool formam uma mistura azeotrópica cujo ponto de ebulição é constante, mas esse fato não permite identificar a diminuição do volume quando ocorre a mistura das substâncias.