Questão 71
(UNESP - 2016 - 1ª FASE)
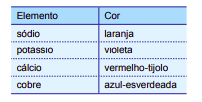
A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade, o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na região da radiação visível, é possível identificar diferentes elementos químicos por meio dos chamados testes de chama. A tabela apresenta as cores características emitidas por alguns elementos no teste de chama:
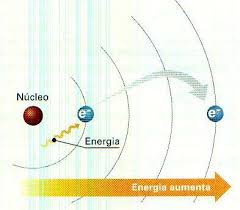
Em 1913, Niels Bohr (1885-1962) propôs um modelo que fornecia uma explicação para a origem dos espectros atômicos. Nesse modelo, Bohr introduziu uma série de postulados, dentre os quais, a energia do elétron só pode assumir certos valores discretos, ocupando níveis de energia permitidos ao redor do núcleo atômico. Considerando o modelo de Bohr, os diferentes espectros atômicos podem ser explicados em função
do recebimento de elétrons por diferentes elementos.
da perda de elétrons por diferentes elementos.
das diferentes transições eletrônicas, que variam de elemento para elemento.
da promoção de diferentes elétrons para níveis mais energéticos.
da instabilidade nuclear de diferentes elementos.
Gabarito:
das diferentes transições eletrônicas, que variam de elemento para elemento.
Resolução:
Cada elemento possui um número de elétrons e cada um desses elétrons tem determinada quantidade de energia. Quando um elétron de uma camada mais interna recebe certa quantidade de energia ele salta para uma camada mais externa sendo denominado estado excitado do elétron. Ao retornar para a sua camada de origem ele libera a energia absorvida em forma de luz o que constitui característica para cada elemento, já que cada energia liberada será emitida em cores diferentes. Esse salto que o elétron faz é chamado de transição eletrônica ou salto quântico como mostra a figura. Portanto. LETRA C.