Questão 22
(UNICAMP - 2022)
Recentemente, pesquisadores desenvolveram uma célula eletroquímica que usa glicose como combustível para gerar eletricidade (figura ao lado). Na célula usam-se enzimas adsorvidas em eletrodos de papel, onde ocorrem as reações que geram a corrente elétrica. O eletrodo da esquerda é previamente mergulhado em solução de glicose ( mol/L) e, depois de retirado dessa solução, a célula está pronta para funcionar. No seu funcionamento (no gráfico, no campo de resposta), observa-se uma queda da corrente ao longo do tempo, um reflexo da diminuição da concentração da glicose. Assim, para efeito de cálculo, podese considerar que a intensidade da corrente elétrica é diretamente proporcional à concentração de glicose.
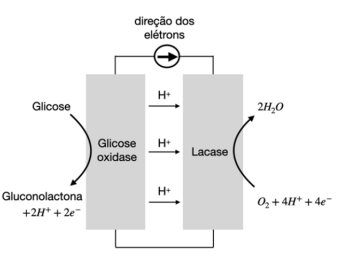
a) Imagine uma situação em que esta célula eletroquímica esteja inserida diretamente na corrente sanguínea de um indivíduo saudável, cuja concentração de glicose é 90 mg/dL. No gráfico do espaço de resposta, esboce a curva da corrente em função do tempo, produzida pela célula nesta situação. Construa a curva, usando argumentos quantitativos, e justifique seu formato.
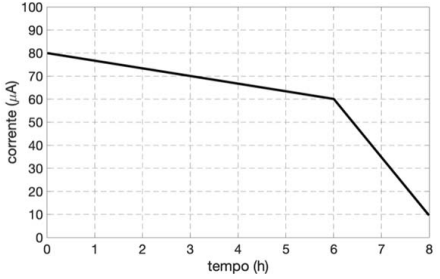
b) Com base nas informações do gráfico disposto no espaço de resposta, calcule a quantidade, em mol de glicose, que foi consumida durante as primeiras 3 horas de funcionamento.
Dado: massa molar da glicose = 180 g/mol. Constante de Faraday: 96500 C/moL (1 C = Aꞏs)
Gabarito:
Resolução:
a)
Para calcular a concentração em quantidade de matéria de solução por volume de solução divide-se a concentração em mg/dL pela massa molar de glicose:
o prefixo d corresponde à 10-1. Isto é, 1dL é igual a 0,1L. Portanto, para expressar a concentração em mmol/L multiplica-se o valor calculado por 10 (ou divide-se por 0,1):
Da situação descrita no enunciado, conclui-se que a solução de concentração 20mmol/L gera uma corrente inicial de 80µA. Como a corrente e a concentração são diretamente proporcionais, pode-se calcular a corrente gerada pela solução de concentração 5mmol/L através da proporção
| 20mmol/L | __________ | 80µA |
| 5mmol/L | __________ | i |
Também a partir da análise do gráfico fornecido, observa-se que a cada 6 horas a corrente decai 25% e neste ponto há uma mudança na inclinação da reta. Portanto, tendo passado 6h, a corrente de 20µA decairá para 15µA.
O esboço da curva deve ter i = 20µA quando t = 0 e i = 15µA quando t = 6h . Essa curva está representada em vermelho na imagem abaixo:
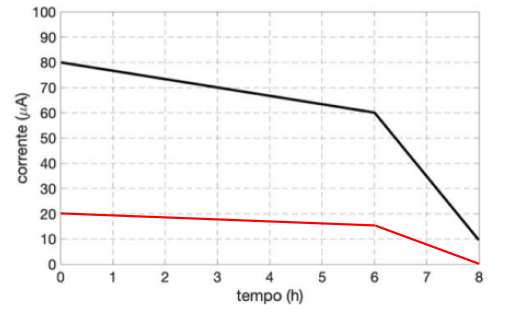
b) A partir do gráfico fornecido, observa-se que no tempo de 3h a corrente decai de 80µA para 70µA. A partir dessa informação, calcula-se a corrente média nesse intervalo de tempo:
A quantidade total de carga pode ser calculada pela multiplicação entre a corrente média (em µA) e o tempo decorrido (em segundos. Para isso multiplica-se o tempo em horas por 3600):
A oxidação de 1mol de glicose libera 2mol de elétrons, como representado pela equação no esquema do enunciado e também pela equação da reação abaixo:
Glicose → Gluconolactona + 2 H+ + 2e-
A quantidade de matéria de glicose consumida no período de 3 horas pode ser calculada a partir da constante de Faraday:
| 96500 C x 2mol | __________ | 1mol |
| 0,810 C | __________ | n |