Questão 15
(UNICAMP - 2023 - 2ª fase)
O concreto tem alta tendência a formar fissuras que reduzem sua vida útil e elevam custos de reposição. A autocura do concreto convencional é o preenchimento de suas fissuras, o que ocorre a partir da hidratação do óxido de cálcio presente na composição do próprio concreto. A hidratação produz hidróxido de cálcio, que reage com o dióxido de carbono presente na atmosfera ambiente. O bioconcreto, um novo produto no mercado, é caracterizado pela presença de bactérias cujas cargas negativas em sua superfície atraem íons metálicos positivos que precipitam com ânions do ambiente do concreto; forma-se, com isso, um sólido pouco solúvel, responsável por fechar as fissuras (figura ao lado).
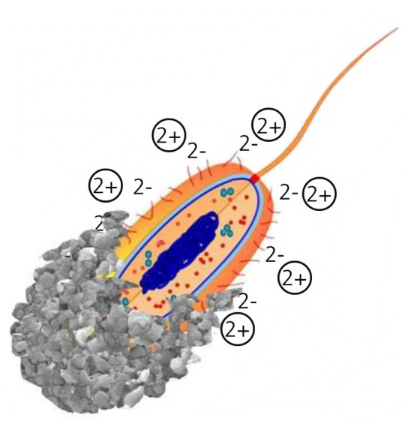
a) A partir do texto acima, equacione os processos químicos descritos na autocura do concreto convencional. Forneça o nome do produto que promove a reparação das fissuras e comente sobre sua solubilidade em água.
b) Em relação aos ânions do ambiente na autocura do bioconcreto, um texto científico relata: “Em pH mais alto, as espécies carbonatadas estão desprotonadas. Como resultado, mais carbonato está disponível para precipitação. Da mesma forma, o grupo fosfato
estará sujeito a mudanças na protonação, dependendo do pH do meio. O grupo sulfato
normalmente estará desprotonado devido aos seus baixos valores de pKa. Assim, a precipitação em pH baixo é possível, mas se aplica, no ambiente do concreto, principalmente ao fosfato e ao sulfato.” Equacione os equilíbrios ácido-base em que, necessariamente, apareçam esses ânions. Comente comparativamente os valores de pKa do ácido associado ao carbonato com os ácidos associados ao sulfato e ao fosfato.
Gabarito:
Resolução:
a) Os processos químicos descritos na autocura do concreto convencional:
O nome do produto que promove a reparação das fissuras e sua solubilidade em água:
O sal carbonato de cálcio é quem promove o preenchimento das fissuras, e o mesmo é pouco solúvel em água.
b) Os valores de pKa do ácido associado ao carbonato com os ácidos associados ao sulfato e ao fosfato.
Quanto maior o valor de Ka menor o valor de pKa e consequentemente mais forte é o ácido.
De acordo com o texto, o ânion CO32- está disponível em valores de pH mais elevados, enquanto os ânions sulfato SO42- e fosfato PO43- estão disponíveis em valores de pH menores.
Portanto, o ácido HSO4- e o HPO42- são ácidos mais fortes, que consequentemente apresentam maiores valores de Ka, enquanto o ácido HCO3- possui menores valores de Ka.
Com isso, o pKa do HCO3- é maior que do HSO4- e o HPO42-