Questão 9405
(UNIFESP - 2005)
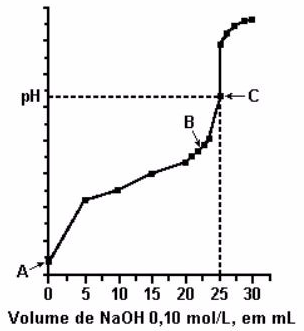
Os resultados da titulação de 25,0 mililitros de uma solução 0,10 mol/L do ácido CH3COOH por adição gradativa de solução de NaOH 0,10 mol/L estão representados no
gráfico.
Com base nos dados apresentados neste gráfico foram feitas as afirmações:
I. O ponto A corresponde ao pH da solução inicial do ácido, sendo igual a 1.
II. O ponto B corresponde à neutralização parcial do ácido, e a solução resultante é um tampão.
III. O ponto C corresponde ao ponto de neutralização do ácido pela base, sendo seu pH maior que 7.
É correto o que se afirma em
I, apenas.
II, apenas.
I e II, apenas.
II e III, apenas.
I, II e III.
Gabarito:
II e III, apenas.
Resolução:
Através do gráfico:
Vamos analisar as alternativas:
I. O ponto A corresponde ao pH da solução inicial do ácido, sendo igual a 1.
INCORRETO. Estamos lidando com o ácido acético, um ácido fraco que não se ioniza completamente. A sua concentração é de 0,1 molL-1 e, por não se ionizar completamente, não teremos liberação de [H+] = 0,1 molL-1. Por isso, o seu pH não será igual a 1 pela fórmula:
II. O ponto B corresponde à neutralização parcial do ácido, e a solução resultante é um tampão.
CORRETO. Em B temos um neutralização parcial do ácido CH3COOH, formando o:
Como houve uma neutralização parcial, teremos a mistura CH3COO-Na+ e CH3COOH, uma solução tampão.
III. O ponto C corresponde ao ponto de neutralização do ácido pela base, sendo seu pH maior que 7.
CORRETO. O pH é maior do que 7, por se tratar de um ácido fraco e uma base forte, formando um sal de caráter básico.