Questão 70584
(UVV - 2018)
O diabetes mellitus consiste em uma síndrome metabólica, caracterizada por níveis elevados de glicose sanguínea (hiperglicemia), causados pela resistência à ação ou pela deficiência na secreção do hormônio insulina. Dados divulgados pela International Diabetes Federation apontam que, aproximadamente, 387 milhões de pessoas são afetadas por essa doença, o que representa uma prevalência de 8,3% na população mundial, caracterizando uma grave epidemia global. Como alternativas terapêuticas sintéticas, destacam-se, entre outros, os compostos orgânicos da classe das biguanidas, sendo a Metformina o fármaco de primeira escolha para uso contínuo, por via oral, em pacientes com diabetes tipo II.
(CONCEIÇÃO, R. A.; SILVA, P. N.; BARBOSA, M. L. C. Fármacos para o Tratamento do Diabetes Tipo II: uma visita ao passado e um olhar para o futuro. Revista Virtual de Química, vol. 9, n. 2, pg. 514-534, 2017.
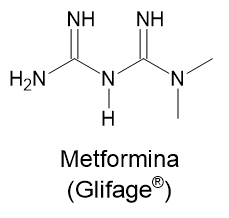
Com base em sua estrutura química, pode-se afirmar que a Metformina:
É um ácido de Brönsted-Lowry, porque possui um átomo de nitrogênio capaz de doar um par de elétrons para uma base.
É um ácido de Lewis, porque possui um átomo de nitrogênio capaz de receber um par de elétrons de uma base.
É uma base de Lewis, porque possui um átomo de nitrogênio capaz de receber um par de elétrons de um ácido.
É uma base de Lewis, porque possui um átomo de nitrogênio capaz de doar um par de elétrons para um ácido.
É um ácido de Brönsted-Lowry, porque possui um átomo de nitrogênio capaz de receber um par de elétrons para uma base.
Gabarito:
É uma base de Lewis, porque possui um átomo de nitrogênio capaz de doar um par de elétrons para um ácido.
Resolução:

a) Incorreto. É um ácido de Brönsted-Lowry, porque possui um átomo de nitrogênio capaz de doar um par de elétrons para uma base.
Ácidos de Bronsted doam prótons para base e não par de elétrons.
b) Incorreto. É um ácido de Lewis, porque possui um átomo de nitrogênio capaz de receber um par de elétrons de uma base.
O átomo de nitrogênio possui par de elétrons para ser doado, portanto, não pode receber par de elétrons.
c) Incorreto. É uma base de Lewis, porque possui um átomo de nitrogênio capaz de receber um par de elétrons de um ácido.
Bases de Lewis doam par de elétrons, e não recebem. O átomo de nitrogênio possui par de elétrons para ser doado, portanto, não pode receber par de elétrons.
d) Correto. É uma base de Lewis, porque possui um átomo de nitrogênio capaz de doar um par de elétrons para um ácido.
O átomo de nitrogênio possui par de elétrons para ser doado, sendo então uma base de Lewis.
e) Incorreto. É um ácido de Brönsted-Lowry, porque possui um átomo de nitrogênio capaz de receber um par de elétrons para uma base.
Ácidos de Bronsted doam prótons para base e não recebem par de elétrons.