Questão 8901
(EsPCEx - 2010)
Considere o gráfico abaixo da reação representada pela equação química:
N2(g) + 3H2(g) 2NH3(g)
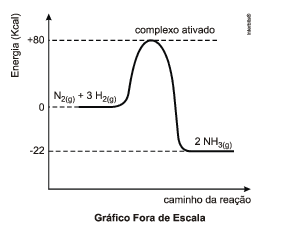
Relativo ao gráfico envolvendo essa reação e suas informações são feitas as seguintes afirmações:
I. O valor da energia envolvida por um mol de NH3 formado é 22 kcal.
II. O valor da energia de ativação dessa reação é 80 kcal.
III. O processo que envolve a reação N2(g) + 3H2(g) 2NH3(g) é endotérmico.
Das afirmações feitas, está(ão) correta(s)
apenas III.
apenas II e III.
apenas I e II.
apenas II.
todas.
Gabarito:
apenas II.
Resolução:
I. Incorreto. O valor da energia envolvida por um mol de NH3 formado é 22 kcal.
Contudo, esse foi calculado para a reação: N2(g) + 3H2(g)
2NH3(g), em que são formados 2 mols de NH3, e não 1 como foi pedido.
A energia da formação de 1 mol de NH3 é -11Kcal
II. Correto. O valor da energia de ativação dessa reação é 80 kcal.
O complexo ativado é formado quando a energia de ativação é atingida, no caso vemos no gráfico 80Kcal.
III. Incorreto. O processo que envolve a reação N2(g) + 3H2(g) 2NH3(g) é endotérmico.
Como , um valor negativo, a reação é exotérmica, ocorre liberação de energia.
Gabarito alternativa D.