Questão 2
(EsPCEx - 2014)
O fosgênio é um gás extremamente venenoso, tendo sido usado em combates durante a Primeira Guerra Mundial como agente químico de guerra. É assim chamado porque foi primeiro preparado pela ação da luz do sol em uma mistura dos gases monóxido de carbono (CO) e cloro 2 (C2 ), conforme a equação balanceada da reação descrita a seguir: CO(g) + C
2(g)
COC
2(g) .
Considerando os dados termoquímicos empíricos de energia de ligação das espécies, a entalpia da reação de síntese do fosgênio é
Dados:

+ 522 kJ/mol
- 78 kJ/mol
- 300 kJ/mol
+ 100 kJ/mol
- 141 kJ/mol
Gabarito:
- 78 kJ/mol
Resolução:
A reação de síntese do fosgênio é:
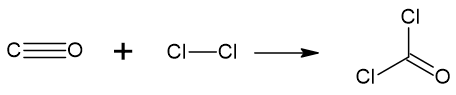
Para descobrir a entalpia dessa reação, devemos analisar as ligações que foram quebradas e formadas durante a reação:
Em que LF são as ligações formadas e LQ as ligações quebradas.
► Ligações Formadas:
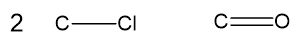
► Ligações Quebradas:

A entalpia da reação será: