Questão 1
(EsPCEx - 2016) O cobre metálico pode ser oxidado por ácido nítrico diluído, produzindo água, monóxido de nitrogênio e um sal (composto iônico). A reação pode ser representada pela seguinte equação química (não balanceada):
Cu(s) + HNO3(aq) → H2O(l) + NO(g) + Cu(NO3)2(aq)
A soma dos coeficientes estequiométricos (menores números inteiros) da equação balanceada, o agente redutor da reação e o nome do composto iônico formado são, respectivamente,
Gabarito:
20, Cu, nitrato de cobre II.
Resolução:
A variação do NOX dessa reação é:
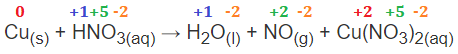
Portanto, o cobre oxida de Cu para Cu+2, e o nitrogênio reduz de + 5 para +2. Para prosseguir com o balanceamento, analisamos a variação de Nox da redução e da oxidação:
ΔNox(oxidação) = 2
ΔNox(redução) = 3
A variação de nox da redução é o coeficiente estequiométrico da oxidação:
3 Cu(s) + HNO3(aq) → H2O(l) + NO(g) + 3 Cu(NO3)2(aq)
A variação de nox da oxidação é o coeficiente estequiométrico da redução, lembrando que nesse caso precisa ser do NO já que é ele que participa da oxidação:
3 Cu(s) + HNO3(aq) → H2O(l) + 2 NO(g) + 3 Cu(NO3)2(aq)
Prosseguindo com o balanceamento por tentativa, a reação balanceada será:
3 Cu(s) + 8 HNO3(aq) → 4 H2O(l) + 2 NO(g) + 3 Cu(NO3)2(aq)
A soma dos coeficientes estequiométricos é 20 (3 + 8 + 4 + 2 + 3 = 20).
O agente redutor dessa reação é o cobre, já que oxida promovendo a redução do nitrogênio.
E o nome do produto Cu(NO3)2 é nitrato de cobre II, já que o ânion NO3- é o nitrato e a carga do cobre é +2.